
���m�点
�y�v���X�����[�X�z �R������Âɔ����f���C��q�f�̌y�����ʂ��m�F �`��t�����E�ɔ��M�����������ʁ`
2016�N07��14��
�y�|�C���g�z
�E������L���a�@��ܕ� ������ ��،����2010�N�A�S���̖�t�ɑ��{�����ōs�����f��Ɋւ����V���Տ������iTRIPLE �����j�ւ̎Q�����Ăт����A���������20�{�݂̋��͂ɂ�莎�����J�n���܂����B
�E���̂��ю����������I�������̌������ʂ��A������厏�u Annals of Oncology �v��2016�N6��29���t�Ō��J����܂����B
�E���̌����́A����܂ł̗Տ������Ƃ͈قȂ�A��t�̎w���̂��ƁA�e�{�݂̖�t�������ƂȂ�A���҂ւ̐����A�]���A����p�⌟���l�`�F�b�N�ACRF�쐬�Ȃǎ����Ɋւ����ȋƖ����t���S���܂����B
�ECDDP���^�㐔���ԑJ������f���C��q�f�ɑ��A�p���m�Z�g�������g�p���邱�Ƃŏ]���̖�܂����y���ł��邱�Ƃ��킩��܂����B
�y�����T�v�z
�x����A�݂���A���z������ȂǂŔėp����Ă���V�X�v���`�� ( CDDP ) ���W�����́A���x�Óf���iHEC: higly emetogenic chemotherapy �j�ɊY�����A���{�����Êw��甭������Ă��鐧�f��K���g�p�K�C�h���C���ɂ����āA5HT3��e�̝h�R��(5HT3RA)�A�j���[���L�j��1��e�̝h�R��(NK1RA)�A�f�L�T���^�]��(DEX)��3�ܕ��p�W�����f�Ö@���{�s���邱�Ƃ���������Ă��܂��B���̂����A5HT3RA�Ɋւ��Ă�2010�N�ɁA�]���̖�܂Ƃ͈قȂ��������Ԃ̍�p��L���鏉�߂Ă̖�܂Ƃ��āA�p���m�Z�g��������������܂����B�������Ȃ���]����5HT3RA�ɔ�����ł����A�����Ďg�p�������߉Ȋw�I���������E�I�ɖR�����ł���܂����B���̂���TRIPLE�����ɂ����āA���E�ŏ��߂�3�ܕW�����f�Ö@�ɂ�����A�O���j�Z�g�����ɑ���p���m�Z�g�����̗L�������m�F�ł��܂����B���Ɏ��ÊJ�n��̐����ԑJ�����鈫�S�q�f���y��������ʂɗD��Ă���ACDDP�ɂ�鎡�Â�����܂ł��͊y�Ɏ���\��������܂��B�i���ҌX�̔w�i��A���^����R�����ɂ���Ă͏]���̖�܂ł��\���ȏꍇ������܂��B�j
�yTRIPLE�����g�D�z
�@�@������\��t�@�@�R�{�M�V�i�a�̎R������ȑ�w��w�����Ȋw��O�u�������j
�@�@�@�@�@�@�@�@�@�@�@�@�i�O�C�F�É������É�����Z���^�[���@�����ċz����ȕ����j
�@�@���������ǁ@�@�@��،���i���L���a�@�@��ܕ��@����ܕ����j
�@�@�@�@�@�@�@�@�@�@�@�@�i�O�C�F�É������É�����Z���^�[��ܕ��j
�@�@���v��͐ӔC�ҁ@�R���|�t�i���l�s����w��w���Տ����v�w���������j
�v���g�R���ψ��@�㓡����i���������Z���^�[���a�@�@�ċz����Ȓ��j
�@�����q�i���������Z���^�[���a�@�@��ܕ��j
�@�@�ց@���F�i�鋞��w��w�������a�@�@�a�@�����j
�@���c�r��i�鋞��w��w�������a�@�@��ܕ��j
�@�����^�c�g�D�@�@���c�@�l���������Y�Ƒn���@�\�t�@���}�o���[�Z���^�[�������i��
�y�����̔w�i�z
2009�N�A���V����w��w���������V����@ ���B�ȋ����@�V�����]��́A50mg/m2�ȏ��CDDP���W���������AC/EC�Ö@��ΏۂƂ��ADEX���p���i �j���[���L�j���P��e�̝h�R��F�ȉ�NK1RA �j�ɂ�����A�O���j�Z�g����( granisetron : �ȉ� GRA )3mg �ƃp���m�Z�g����( palonosetron : �ȉ�PALO ) 0.75 mg�̌��ʂ��A��d�ӌ������_������r�����ɂ�茟�����܂����i PROTECT study �j1�B���̌��ʁA�S���� ( CDDP���^��0�`120���Ԉȓ� )��CR����PALO 47.9���AGRA 38.1���ip��0.0007�j�A�x�����ɂ����Ă�PALO 53.0���AGRA 42.4���ip��0.0003�j�ƁAPALO�Q�͗L���ł��邱�Ƃ��ؖ�����܂����B�܂��u���S�Ȃ��v �̊����ɂ����Ă����l�ɑS���ԁi PALO 31.9���AGRA 25.0%�Fp��0.0117 �j�A�x�����iPALO 37.8���AGRA 27.2%�Fp��0.0002 �j�Ƃ���PALO ��GRA �ɑ���D�z�����ؖ�����܂����B���̂��Ƃ���A�����̐��f�Ö@�K�C�h���C���ł͒����x�Óf�����X�N���w�Ö@�iModelately Emetogenic Chemotherapy �ȉ��FMEC�j�ɂ�����2-4�A�܂��ꕔ�̃K�C�h���C���ł�HEC�ɂ����Ă�5HT3RA�Ƃ���PALO�̎g�p����������Ă��܂�4�B�������Ȃ���A���݁A���{�����Êw��̐��f��K���g�p�K�C�h���C���ł�HEC�ɂ����āANK1RA�̕��p����������Ă��܂����ANK1RA���p���ɂ����Ă��APALO��GRA�����D��Ă��邩�ǂ����́A������ɂ�����ꂽ�݂̂ł���A�Ȋw�I�ȍ����ɖR�����ł����B�{�����ł�NK1RA�A����уK�C�h���C���Ő�������Ă���p�ʂ�DEX���p���ɂ����āi�W�����f�Ö@�jGRA�ɑ���PALO�̗L�����������܂����B���̌������ʂ�CDDP�ȂǍÓf���̍������W�����ɑ���A�����Ƃ��L���Ȑ��f�Ö@���m�����邱�ƂɂȂ��邽�߁A�����ւ�L�v�ƍl���Ă��܂��B
�����ʼn�X�͌Ō`��ᇂɑ�CDDP�x�[�X��HEC�{�s�\�芳�҂�ΏۂƂ��ADEX�����APR ( NK1RA )���܂�3�ܕ��p���f�Ö@�ɂ�����AGRA�ɑ���PALO�̐��f���ʂ������邽�߂ɁA�S��20�{�݂̖�t�����S�ƂȂ�A��t��̋��͂ȃT�|�[�g�̂��Ɠ�d�ӌ��������r�����i ���{������V������ : TRIPLE study �j�����{���܂����B
�y�����̓��e�z
���҂͓��{������20�{�݂��A�{�����ɓo�^����܂����B�Ώۂ́A���ÂƂ���CDDP(��50mg/m2)���܂�HEC���{�s�����\��̌Ō`��ᇊ��҂Ƃ��܂����B���Q�Ƃ���APR��CDDP���^60���O��125mg�A��2���ځA3���ڂ�80mg���������^����ADEX��CDDP���^�O��9.9mg (i.v.)�A�� 2���ځ`4���ڂ�6.6mg (i.v.)�����^����܂����B������͊e�{�݂̒��ܒS����t�����ۓI�ɒ������s������A�ӌ���t���a���ɂďǏ�]�����s���܂����B�Ȃ��A�{�����͏Ǐ��]��������t�̑��A�W�������ׂĂ̈�t����ъŌ�t�A���Җ{�l�A��v�S���҂��ӌ������ꂽ��ԂŎ��{����Ă���A�W�X�^�b�t�̜��ӓI�ȉe���͋ɂ߂ĒႢ�̂��Ǝ��{����܂����B�܂��{�����́A�ŏ����@��p���Ċ��t���s���A���t�������q�͎{�݁A�N��i<60�A��60�j�A���ʁACDDP���^�ʁi<70mg/m2�A��70mg/m2�j�Ƃ��܂����B�ώ@���Ԃ�CDDP���^�J�n��120���Ԍo�ߌ�܂łƂ��Ă��܂��B�����f�U�C����}�P�Ɏ����܂��B
�}1
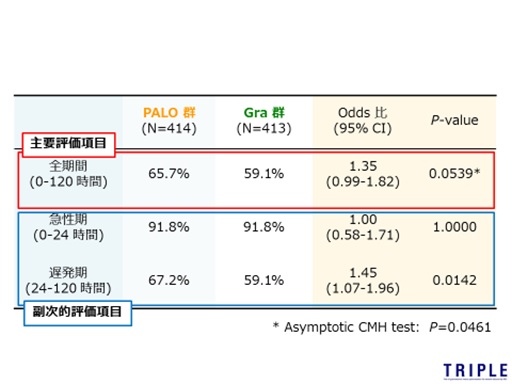
�y�������ʁz
��v�]�����ځiCR���j
�ECR���Fcomplete response �q�f���S�}�����i�q�f�Ȃ��A�lj��̐��f�p�Ȃ��̊����j
PALO�Q�AGRA�Q�̑S����CR���͂��ꂼ��65.7���A59.1���ł���A���̍��͂����킸���ł͂��邪���v�w�I��PALO��GRA�ɑ���D�z���������ɂ͎���܂���ł����i OR 1.35 95��CI 0.99-1.82 : p��0.0539 �j�B�}������CR���͂ǂ����5HT3RA��p���Ă�91.8���ƍ���CR�����m�F�ł��A��s�����Ɠ��l�ɗǍD�Ȍ��ʂƂȂ�܂����B����x������CR���ł�PALO�Q��GRA�Q�ł͂��ꂼ��68.2���A59.1����PALO�Q�ɂ����ėL���Ȑ��т� ( p=0.0142)���m�F����܂����B
�\1
�����]�����ځiCC���ATC���j
�ECC���Fcomplete control
�i�q�f�Ȃ��A�lj��̐��f��Ȃ��A���S�y�x�܂��͖����̊����j
�ETC�� : total control
�@�i�q�f�Ȃ��A�lj����f��Ȃ��A���S�Ȃ��̊����j
���Q�̑S����CC����PALO 63.8%,�AGRA 55.9%�A�S����TC���ł�PALO 47.6 %�AGRA 40.7 % �ł����B�܂��ACR���Ɠ��l�ɒx�����ɂ����Ă��̍��͂�茰���ł���ACC����9.3�� ( PALO 65.2% : GRA 55.9% )�ATC����7.2�� ( PALO 48.6% : GRA41.4% )�̏�悹���ʂ��F�߂��܂����B�i�}2�j
�@��Ȏ�����֘A�̗L�Q���ۂ͕֔�ł���PALO�Q�� 52.3%�AGRA�Q��51.1%�ɔF�߂��܂����B���̑��h�t�A�������Ȃǂ��F�߂��܂������A���Q�Ԃ̔������A�d�ēx�ɍ��͂Ȃ��X�Ɏ�����Ɋ֘A�����O���[�h4�ȏ�̏d�ĂȗL�Q���ۂ͔F�߂��܂���ł����i�\2�j
�}2

�\2
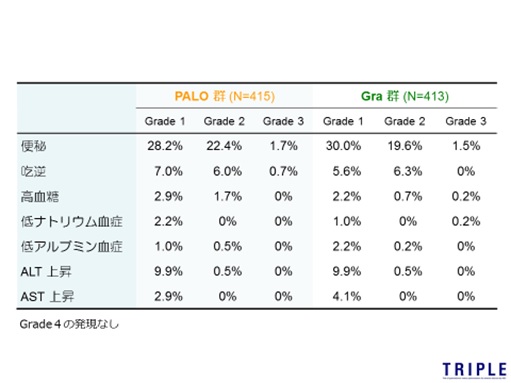
�y�܂Ƃ߁z
CDDP���W�����{�s���̈��S�q�f�\�h��Ƃ��āA�{�M�ł͍�p�@���̈قȂ�3�ܕW�����f�Ö@����������Ă��܂��B���̂�����5HT3RA�Ƃ��ẮAPALO��p���邱�ƂŒx�����̈��S�q�f�A����ёS���Ԃ̈��S�ɑ���L�������ؖ�����܂����BPALO��GRA���������ȁi4-5�{�j��܂ł���A��p�Ό��ʂ̊ϓ_����͋c�_�̗]�n�����邩������܂���B�������Ȃ���A���w�Ö@�́A�J��Ԃ����^����邱�Ƃ������A���Â��畛��p��\�h���邱�ƂŁA�H���ێ�ʒቺ�ɂ��R�����̌��ʂ�A���Ò��~�Ȃǂ�����ł���\��������܂��B����p�𗝗R�Ƃ����R�����̌��ʂ⒆�~�́A���ʓI�Ɏ��Ì��ʂ���߂�\��������A�\�Ȍ��������邽�߂̍���u���邱�Ƃ��A����̂�����Âł͂����ւ�d�v�Ǝv���܂��B
�y�{�����̎x���z
�{���������c�@�l���������Y�Ƒn���@�\�t�@���}�o���[�Z���^�[�ɂ��A�����^�c����ю����I���������{����܂����B
�y�f�ڂ��ꂽ�_�����z
Randomized , double-blind , phase III trial of palonosetron versus granisetron in the triplet regimen for preventing chemotherapy-induced nausea and vomiting after highly emetogenic chemotherapy : TRIPLE study
�y���p�_�����z
1.�@Saito M, Aogi K, Sekine I, Yoshizawa H, Yanagita Y, Sakai H, et al. PALOnosetron plus dexamethasone versus granisetron plus dexamethasone for prevention of nausea and vomiting during chemotherapy: a double-blind, double-dummy, randomised, comparative phase III trial. The lancet oncology. 2009; 10(2): 115-24.
2.�@Basch E, Prestrud AA, Hesketh PJ, Kris MG, Feyer PC, Somerfield MR, et al. Antiemetics: American Society of Clinical Oncology clinical practice guideline update. Journal of clinical oncology : official journal of the American Society of Clinical Oncology. 2011; 29(31): 4189-98.
3. �@MASCC/ESMO Antiemetic Guideline 2016; �@
http://www.mascc.org/assets/Guidelines-Tools/mascc_antiemetic_guidelines_english_201 6_v.1.1.pdf
4. �@Eisenberg P, Figueroa-Vadillo J, Zamora R, Charu V, Hajdenberg J, Cartmell A, et al. Improved prevention of moderately emetogenic chemotherapy-induced nausea and vomiting with PALOnosetron, a pharmacologically novel 5-HT3 receptor antagonist: results of a phase III, single-dose trial versus dolasetron. Cancer. 2003; 98(11): 2473-82.
�y���₢���킹��z
�i�{�����Ɋւ��邱�Ɓj
���v���c�@�l������L���a�@�@��ܕ��@��،���
�@��135-8550 �����s�]����L���O����8��31��
�@�d�b�@03-3570-0215�@�i�����@7703�j


