研究内容Research
1. 研究戦略
私たちは、2つのアプローチを取っています。- 遺伝子driven 型アプローチ (リバースジェネティクス)
- がんの遺伝子変異は、多くのがん種でデーターベース化されています。しかし、それらががんのドライバーとして機能しているのか、あるいは治療標的分子となりうるのか、など機能的な意義は十分に理解できていません。細胞生物部では、ヒトのがんで見られる遺伝子変異をオルガノイドやマウスに導入し、その生物学的な機能を解析しています。
- 表現型driven 型アプローチ (フォワードジェネティクス)
- がん組織は、増殖能や分化度、あるいは悪性度や薬剤感受性など、患者間で異なる特徴を持っていることが知られています。私たちは、臨床検体から生きた細胞を単離し、その生物学的な特徴を解析し、弱点を探すことにより、新たな治療法の開発に取り組んでいます。
2. 研究プラットフォーム
- 臨床検体由来オルガノイド
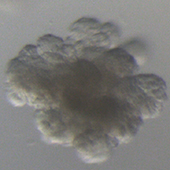 ヒトのがんを組織レベルで解析するために、主に、がん研有明病院との連携により作製された3次元培養組織(オルガノイド)を使っています。大腸がんを中心に、数多くのオルガノイドを樹立し、パネル化を進めるとともに、転移・再発あるいは低分化がんなど特定の現象や病態にフォーカスした研究を行っています。
ヒトのがんを組織レベルで解析するために、主に、がん研有明病院との連携により作製された3次元培養組織(オルガノイド)を使っています。大腸がんを中心に、数多くのオルガノイドを樹立し、パネル化を進めるとともに、転移・再発あるいは低分化がんなど特定の現象や病態にフォーカスした研究を行っています。
- 遺伝子改変マウス
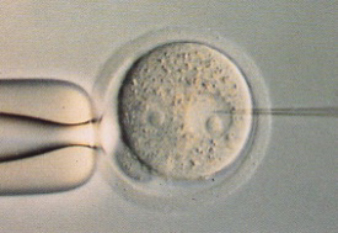 個体レベルの解析では、がんモデルマウスを用いています。すでに樹立されている遺伝子改変マウスに加え、ゲノム編集により新たな変異を導入することにより、詳細な解析をしています。遺伝子改変マウスは、本来の組織に生じる自然発症の腫瘍を個体レベルで解析できる点が大きなメリットです。
個体レベルの解析では、がんモデルマウスを用いています。すでに樹立されている遺伝子改変マウスに加え、ゲノム編集により新たな変異を導入することにより、詳細な解析をしています。遺伝子改変マウスは、本来の組織に生じる自然発症の腫瘍を個体レベルで解析できる点が大きなメリットです。
3. 具体的なプロジェクト
- がん組織の細胞多様性・可塑性の解明
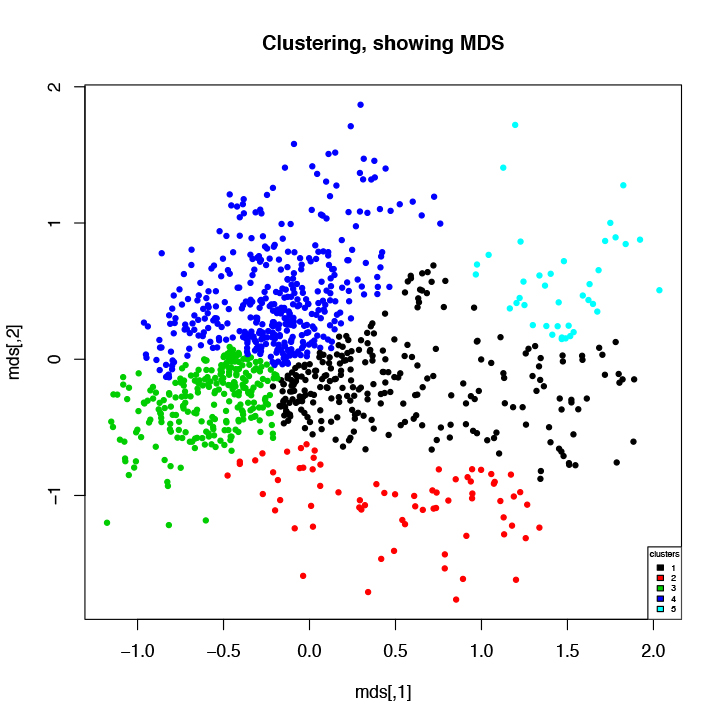 ヒト臨床検体由来オルガノイドの1細胞解析(scRNA-seq, scATAC-seqなど)を行い、がん組織を構成する細胞集団の同定を行っています。これらの結果に基づいて、ゲノム編集によるがん幹細胞の可視化や除去実験を行い、細胞階層性や可塑性の制御機構の解明に取り組んでいます。
ヒト臨床検体由来オルガノイドの1細胞解析(scRNA-seq, scATAC-seqなど)を行い、がん組織を構成する細胞集団の同定を行っています。これらの結果に基づいて、ゲノム編集によるがん幹細胞の可視化や除去実験を行い、細胞階層性や可塑性の制御機構の解明に取り組んでいます。
- がん化学療法の開発
 がんの治療を目的として、分子治療標的薬をはじめとする、様々な薬剤が開発されています。私たちは、新しい治療標的分子の阻害剤の評価に加え、抵抗性や再発など、多数の克服すべき課題について、臨床検体由来オルガノイドを用いて検討しています。患者さんの治療効果予測に基づく層別化法や新たな治療薬の開発が目標です。
がんの治療を目的として、分子治療標的薬をはじめとする、様々な薬剤が開発されています。私たちは、新しい治療標的分子の阻害剤の評価に加え、抵抗性や再発など、多数の克服すべき課題について、臨床検体由来オルガノイドを用いて検討しています。患者さんの治療効果予測に基づく層別化法や新たな治療薬の開発が目標です。
- がんの転移・再発機構の解明
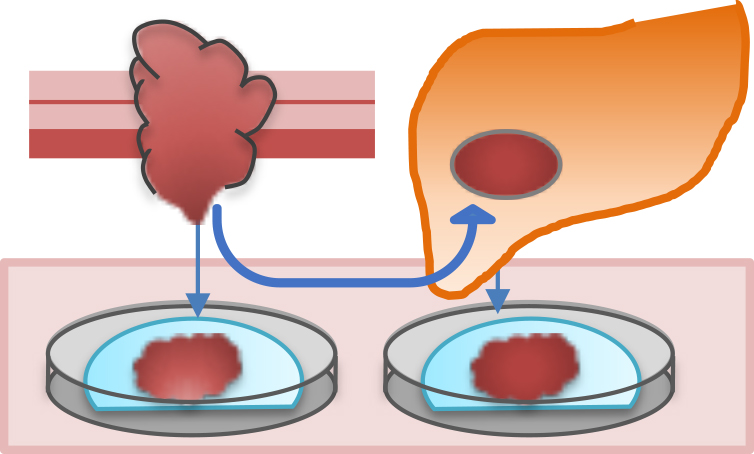 がん治療において、転移と再発は、最大の課題です。同一の患者さんに生じた原発巣、転移巣、再発巣からオルガノイドを樹立し、オミックス解析や同所移植実験、抗がん剤に対する感受性の検討などを行い、がんの転移・再発機構の解明を目指しています。
がん治療において、転移と再発は、最大の課題です。同一の患者さんに生じた原発巣、転移巣、再発巣からオルガノイドを樹立し、オミックス解析や同所移植実験、抗がん剤に対する感受性の検討などを行い、がんの転移・再発機構の解明を目指しています。
- 個体レベルのがんの発生・進展機構の解明
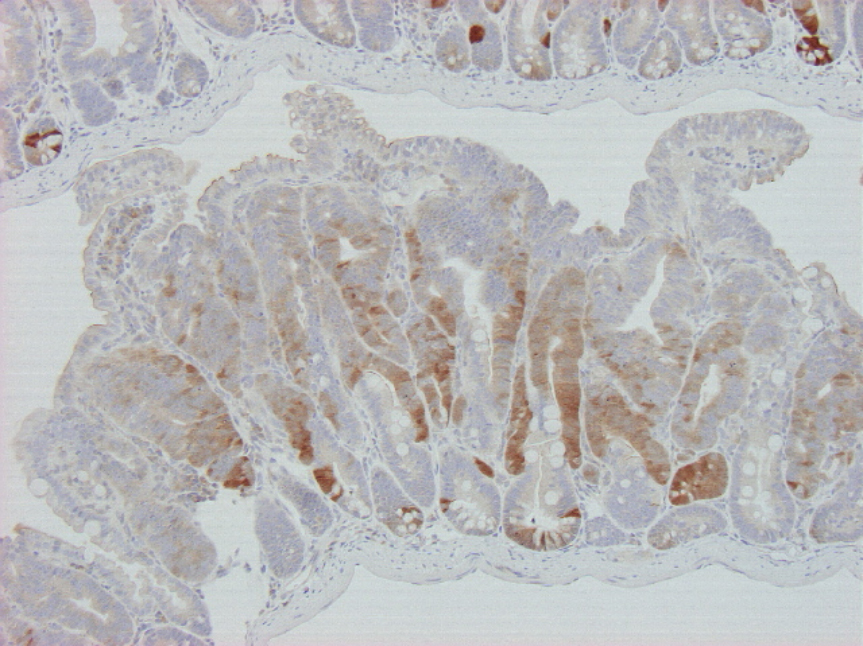 ヒトで生じる遺伝子変異や染色体異常などの遺伝学的な変化をマウスに導入し、がんの発生・進展における機能解析を行っています。CRISPR-Cas9技術の登場により、従来困難であった複雑な解析が可能になっています。
ヒトで生じる遺伝子変異や染色体異常などの遺伝学的な変化をマウスに導入し、がんの発生・進展における機能解析を行っています。CRISPR-Cas9技術の登場により、従来困難であった複雑な解析が可能になっています。
