【プレスリリース】EGFR変異陽性肺がんに対する新規耐性克服療法を発見 〜今後予想されるオシメルチニブ耐性の克服へ〜
2017年03月13日
1.概要
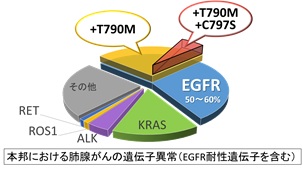
肺がんは我が国において現在がんによる死因の1位であり、さらなる増加が予測されています。EGFR(上皮成長因子受容体)遺伝子変異は進行非小細胞肺がんの3〜4割に見つかりEGFR阻害薬が非常に高い効果を示しますが、1年程度で耐性を生じて再増悪してしまいます。この耐性のおよそ半数を占めるのがEGFR−T790M変異ですが、その耐性変異にも有効なEGFR阻害薬であるオシメルチニブが、日本でも処方可能となりました。しかしさらなる耐性の出現が確認されており、その原因の1つがC797S変異の追加(EGFR-T790M/C797S)であり、臨床応用された全てのEGFR阻害薬の効果がなくなることが報告されています。C797S変異はオシメルチニブ使用中の患者さんのなかで約2割に出現することが報告されており、今後相当数の患者さんで認められることが予想されますが、現在この変異によって再増悪した時の治療法は明確ではありません。
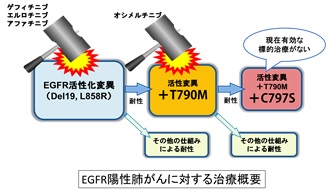
・がん研究会の片山量平らの研究グループは、C797S遺伝子変異によりオシメルチニブに耐性となった細胞に対して、現在ALK阻害薬として開発が進んでいるブリガチニブが有効であることを発見しました。さらに京都大学・理化学研究所との共同研究により、スーパーコンピュータ「京」による構造シミュレーションを行い、ブリガチニブの変異EGFRタンパク質に対する結合様式ならびに、その結合に重要な化学構造の推定に成功しました。
・ブリガチニブとEGFRに対する抗体薬(セツキシマブ、又はパニツムマブ)を併用することで効果が増強されることを見出し、動物実験でも十分な治療効果を確認しました。
・本研究の結果は、オシメルチニブの普及により出現が推定されるC797S遺伝子変異に対する治療開発に貢献しうる成果であると考えられます。
本研究の成果は、英国のNature Publishing Groupオープンアクセス誌Nature Communications(2017年3月13日 英国時間午前10時、日本時間午後7時)に公開されました。
2.ポイント
●EGFR陽性肺腺癌の患者さんにおいて、EGFR阻害剤治療中にT790M耐性変異による増悪がみられた際にはオシメルチニブ(タグリッソ®)を使用することが推奨されており、今後も多くの患者さんがオシメルチニブによる治療を受けることが想定されます。
●オシメルチニブによる治療中に約2割の患者さんにおいてC797S変異が新たに出現してしまうことでオシメルチニブが無効になることが報告されていますが、この耐性に対する有効な分子標的治療は確立していません。
●本研究から、オシメルチニブ耐性となりC797S変異が確認された場合に、ALK阻害薬ブリガチニブとEGFR抗体の併用療法が有効である可能性がありますが、実用化されるためには安全性と有効性を、今後臨床試験により評価する必要があります。
3.論文名、著者およびその所属
○論文名
Brigatinib combined with anti-EGFR antibody overcomes Osimertinib resistance in EGFR-mutated non-small-cell lung cancer
○ジャーナル名
Nature Communications (Nature Publishing Groupのオープンアクセス誌)
(※2017年3月13日英国時間午前10時、日本時間午後7時でオンラインに掲載されています。)
○著者
Ken Uchibori1,2, Naohiko Inase2, Mitsugu Araki3, Mayumi Kamada4, Shigeo Sato1, Yasushi Okuno3,4, Naoya Fujita1, Ryohei Katayama1*
* 責任著者
○著者の所属機関
1.公財)がん研究会 がん化学療法センター 基礎研究部
2.東京医科歯科大学 医歯学総合研究科 統合呼吸器病学
3.理化学研究所 計算科学研究機構 プロセッサ研究チーム
4.京都大学 大学院医学研究科 人間健康科学系専攻ビッグデータ医科学分野
4.研究の詳細
背景と経緯
現在、日本国内において年間7-8万人の方が肺がんが原因で亡くなっていることが公表されていますが、これはがんの部位別死亡者数の1位であり、今後も増加することが予想されています。肺がんはその多くが、残念ながら診断時で手術が適応されない進行がんとして発見されるため、抗がん剤を中心とした薬物治療が治療の中心となっています。非小細胞肺がんは、肺がん全体の85%程度を占めますが、そのなかの30-40%にはEGFR遺伝子に活性型変異が見つかります。こうしたEGFR遺伝子変異が陽性である場合には、この変異を標的とした分子標的薬(ゲフィチニブ:イレッサ®、エルロチニブ:タルセバ®、アファチニブ:ジオトリフ®)が著効することが知られており、従来の殺細胞作用を主とした抗がん剤でおよそ1年程度であった進行肺がんの生存期間中央値を2〜3年へと延長することが確認されています。
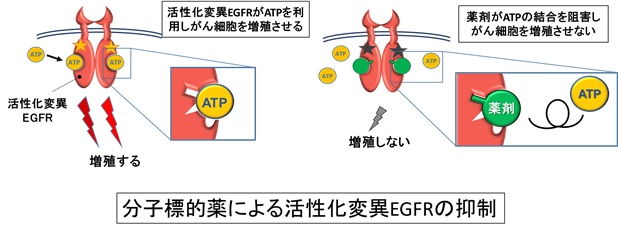
しかしながら、分子標的薬は初期にどれほど高い効果を示したとしても、およそ1年前後で薬が効かなくなる薬剤耐性が生じ、がんは再び増大・進行してしまいます。薬剤が結合する部位が変化する2次変異がこうした分子標的薬への耐性をもたらしますが、特にEGFR-T790M変異が出現して薬剤が働かなくなることが分かっていました。
近年、新たな分子標的薬として、T790M変異が生じても効果を示す薬剤(オシメルチニブ:タグリッソ®)が開発され、日本でも2016年5月から実際に臨床で使用されています。この薬剤が普及することによって、ゲフィチニブなどの最初に用いられる分子標的薬に耐性となった後でもT790M変異が確認できる場合には、オシメルチニブによってさらに長い期間にわたって肺がんを制御して生存期間をより延長できるようになることが期待されます。しかし残念ながら、オシメルチニブに対してもさまざまなメカニズムで耐性が出現することが臨床上明らかになってきており、こうしたオシメルチニブ耐性を克服する手法の開発が必要とされています。オシメルチニブ耐性メカニズムのひとつとして、C797S変異が追加されるものが報告されており、我々はT790M変異に加えてC797S変異を生じることで起こるオシメルチニブ耐性を克服しうる治療法を発見するために研究を進めてきました。
研究内容
IL-3依存的に増殖するマウス前駆Bリンパ球(Ba/F3細胞株)に、活性化変異型EGFRを遺伝子導入することで、IL-3に依存せずにEGFRに依存して生存・増殖するBa/F3細胞を作製し、分子標的薬に対する反応性を検討しました。EGFR活性化変異単独では、前述のゲフィチニブ、アファチニブ、オシメルチニブのいずれもが有効でしたが、T790M変異が加わる(2重変異)とオシメルチニブのみに有効性が認められ、さらにC797Sが追加される(3重変異)とこれらすべての薬剤は効果を示さなくなりました。この3重変異EGFR(C797S/T790M/活性化変異)に対して有効な薬剤を発見するために、現在すでに臨床応用されている、ないしは開発中の薬剤を中心にスクリーニングしたところ、ALK融合遺伝子陽性肺がんに対する治療薬として開発中のALKチロシンキナーゼ阻害薬ブリガチニブが3重変異EGFRに有効であることを見出しました。この薬効は遺伝子導入により人工的に作製した3重変異EGFR 陽性Ba/F3細胞だけでなく、肺がん患者さんの肺がん細胞から樹立された3重変異EGFR陽性細胞においても確認することができています。
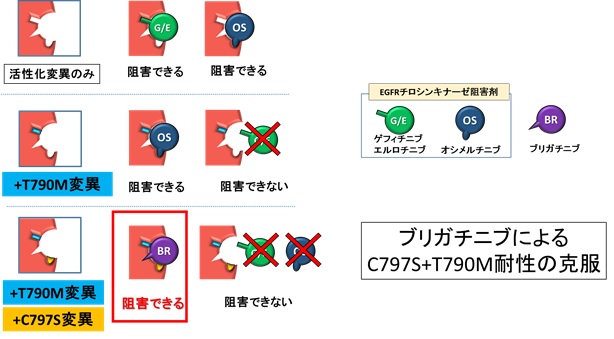
ALK融合遺伝子陽性がんに有効性を期待できるALK阻害薬は、ブリガチニブ以外にも複数のものが存在しているため、それらについても検討を行いましたが、ブリガチニブのみが3重変異EGFRに対して有効性を示したため、この薬効の差異と各阻害薬の構造式を比較し、ブリガチニブのどの構造が3重変異EGFRの阻害活性に寄与しているか同定しました。さらに、京都大学、理化学研究所との共同研究により、スーパーコンピュータ「京」を用いたたんぱく質構造シミュレーションを行うことで、ブリガチニブが3重変異EGFRにどのように結合してその機能を阻害しているか、結合に寄与度の大きい原子はどれかを推定することに成功しました。このことは、将来、より高活性の化合物を合成展開していくうえで重要な情報になると考えられます。
.jpg)
(スーパーコンピュータ「京」による構造シミュレーションにて、ブリガチニブ(緑・水色表示)が3重変異のEGFR(灰色表示)に結合する様子が推定できました)
一方でブリガチニブ単剤では、3重変異EGFRを有する肺がん細胞をマウスに移植して作製した担癌マウスモデルでの動物実験では期待されるほどの抗腫瘍効果を示しませんでした。しかしながら、EGFRに結合しその機能を阻害する抗体(抗EGFR抗体)であるセツキシマブ(アービタックス®)やパニツムマブ(ベクティビックス®)をブリガチニブと併用することでブリガチニブの効果が顕著に高まることを、細胞株、および担癌マウスモデルを用いた実験の結果新たに見出すことに成功しました。さらにブリガチニブは野生型EGFRを阻害する活性が変異型EGFRを阻害する活性に比べ10倍程度弱く、変異型EGFRに選択的に阻害活性を示しました。このことは、ブリガチニブと抗EGFR抗体の併用がEGFRの3重変異によるオシメルチニブ耐性を克服する手段の候補になりうることを期待させる結果でありますが、臨床試験による安全性および有効性の検討が今後必須であると考えられます。
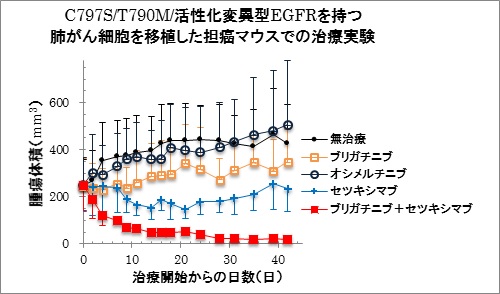
(担癌マウスモデルにてブリガチニブ+セツキシマブが高い有効性を示しました)
研究のインパクトおよび今後の展開
オシメルチニブがT790M変異を有するEGFR変異陽性肺がん患者の治療薬として急速に広く日常診療に浸透している現状から、今後C797Sによる耐性が出現してくることが想定されています。しかし一方で、現在C797Sを克服する薬剤として臨床段階まで開発が進んでいる薬剤は存在しません。本研究で見出したブリガチニブとセツキシマブ、パニツムマブの併用療法については、ブリガチニブがALK陽性肺がんに対する治療薬として第3相臨床試験中であり、セツキシマブおよびパニツムマブは大腸がんや頭頚部がんですでに広く実臨床で使用されています。そのため、全くの新しい治療薬開発に比べ、より早く臨床的な効果や安全性を検証する臨床試験へと繋げられることが期待できます。さらに、本研究で示されたブリガチニブのC797S変異をもったEGFRへの結合部位に関する情報とブリガチニブの誘導体展開可能と考えられる部位に関する情報は、今後、より強力で特異的な治療薬の開発へと展開するのに重要な情報となる可能性があります。
5.本研究への支援
本研究は、下記機関より資金的支援等を受けて実施されました。
・国立研究開発法人日本医療研究開発機構(AMED) 次世代がん医療創生研究事業(P-CREATE)
・独立行政法人日本学術振興会 科学研究費補助金
・公益財団法人車両競技公益資金記念財団
・文部科学省 ポスト「京」で重点的に取り組むべき社会的・科学的課題に関するアプリケーション開発・研究開発 重点課題1 (課題責任者 奥野恭史 博士)
・本論文の一部は、理化学研究所のスーパーコンピュータ「京」を利用して得られたものです。
(課題番号: hp160213, hp150272)
6.用語解説
(注1)EGFR遺伝子変異
EGFR(上皮成長因子受容体)は細胞膜上に発現するチロシンキナーゼ受容体であり、上皮成長因子 (EGF) が結合すると受容体は活性化し、細胞増殖シグナルを活性化することで、細胞を生存・増殖させます。しかし、EGFRの細胞内チロシンキナーゼ領域に特定のアミノ酸の欠失または1アミノ酸変異を起こす遺伝子変異があると、EGFRが恒常的に異常活性化します。それにより細胞増殖シグナルが常時活性化をし、がん化が引き起こされています。EGFR遺伝子変異陽性の肺がん細胞はEGFRのチロシンキナーゼ活性に依存して生存・増殖しているため、EGFRチロシンキナーゼ阻害薬により、EGFRからの細胞増殖シグナルは遮断され、がん細胞の生存・増殖は抑制されます。
(注2) チロシンキナーゼ
キナーゼとは基質をリン酸化する酵素の総称であり、そのうちチロシンキナーゼは基質たんぱくのチロシン残基をリン酸化する酵素のことです。一般にその活性化は私たちの細胞の増殖を正に誘導します。
関連PDF
- プレスリリース文書
 (1,055.4KB )
(1,055.4KB )