- HOME
- 新着情報
【プレスリリース】老化した細胞が鉄で死なない仕組みを解明〜リソソームの酸性度が細胞死の鍵を握る〜
2025年07月29日
1.ポイント
●老化細胞※1では、鉄による細胞死(フェロトーシス)※2が起こりにくいことが知られていましたが、そのメカニズムは不明でした。
●老化細胞が正常な細胞と比較して死ににくい原因は、リソソーム※3の機能不全であることを発見しました。
●老化細胞において、リソソーム内を酸性に保つ働きをもつタンパク質複合体の機能が低下することが明らかになりました。
●老化細胞のリソソームを酸性化させると、リソソーム内に滞留している鉄がリソソーム外に分布するようになり、フェロトーシスに対する感受性が回復することを示しました。
●膵臓がん細胞も老化細胞と同様のリソソーム機能異常を示すことから、リソソームを酸性化させる薬剤によって膵臓がんの発症や進行を抑えられることが分かりました。これにより、リソソームの酸性度を制御することが新しいがん治療の戦略として期待されます。
2.概要
がん研究会がん研究所細胞老化研究部の羅智文(ろーつーうぇん)特任研究員、周翔宇(しゅうしょうう)博士研究員、高橋暁子(たかはしあきこ)部長を中心とするグループは、正常な細胞においては酸性に保たれている細胞内分解器官であるリソソームの内部が老化細胞では中性に近づくことで、老化細胞においてリソソーム内部に鉄が滞留し、鉄依存性の細胞死である「フェロトーシス」が生じにくくなることを明らかにしました。がん研究会がん研究所細胞老化研究部の羅智文(ろーつーうぇん)特任研究員、周翔宇(しゅうしょうう)博士研究員、高橋暁子(たかはしあきこ)部長を中心とするグループは、正常な細胞においては酸性に保たれている細胞内分解器官であるリソソームの内部が老化細胞では中性に近づくことで、老化細胞においてリソソーム内部に鉄が滞留し、鉄依存性の細胞死である「フェロトーシス」が生じにくくなることを明らかにしました。
正常な細胞がさまざまなストレスを受けた結果として生じる老化細胞は、慢性的な炎症環境をつくることで、がんを含む加齢性疾患の発症や進行を促進することが知られています。近年、老化細胞に蓄積した鉄が炎症性因子の誘導や病態の発症に関わることが明らかになりつつあります。興味深いことに、老化細胞は鉄を多量に保持しているにもかかわらずフェロトーシスに対して抵抗性を示すことが報告されていますが、その詳細なメカニズムは不明でした。
本研究グループは、細胞内のリソソームの機能がフェロトーシスの誘導に重要な役割を果たすことを明らかにしました。老化細胞ではリソソームの酸性度を保つV-ATPase※4というタンパク質複合体の機能が低下しているためにリソソーム内部が中性に近くなり、これにより2価鉄イオン(Fe2+)がリソソームに留まることで、フェロトーシスの原因となる脂質過酸化反応※5が細胞全体で生じにくくなることを発見しました。そして、リソソームを酸性化させる薬剤を処置した老化細胞は、フェロトーシスを引き起こしやすくなることを明らかにしました(図)。
図. 老化細胞のリソソームを酸性化させることでフェロトーシス感受性が高くなる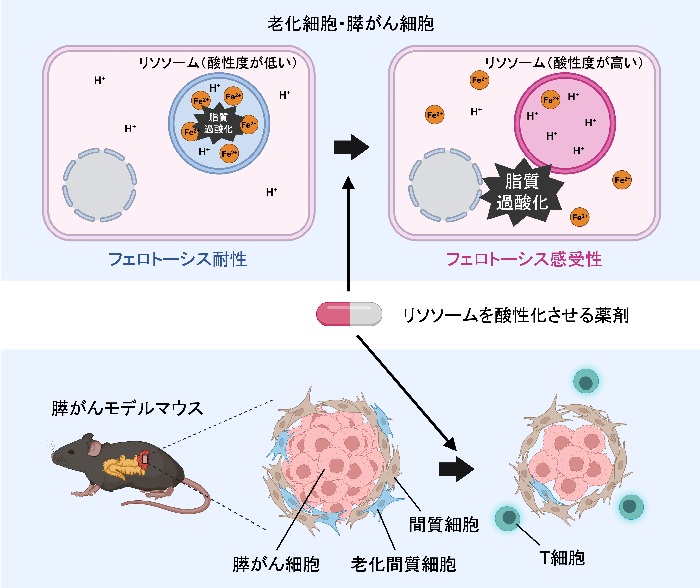
さらに本研究グループは、老化細胞と同様のリソソーム機能異常が膵臓がん細胞でも起こって、がん細胞のフェロトーシス抵抗性にも関与していることを見出しました。膵臓がんのモデルマウスを用いた実験で、リソソームの酸性化によって膵臓がんの発症やがん細胞の増殖を抑制できることを示しました(図)。本研究により、老化細胞におけるリソソーム機能障害とフェロトーシス抵抗性との関連が明らかになったことで、リソソームの酸性度を制御することが、がんを含む加齢関連疾患の新たな治療戦略となる可能性が示唆されました。
本研究成果は、令和7年7月29日18時(日本時間)に、Nature Communicationsオンライン版に掲載されます。
3.論文名、著者およびその所属
論文名
Senescence-associated lysosomal dysfunction impairs cystine deprivation-induced lipid peroxidation and ferroptosis
ジャーナル名
Nature Communications
著者
Tze Mun Loo1, Xiangyu Zhou1, Yoko Tanaka1, Sho Sugawara1, Shota Yamauchi1, Hiroko Kawasaki1, Yuta Matsuoka2, Yuki Sugiura2, Shinya Sakuma3, Yoko Yamanishi3, Satoshi Yotsumoto4, Kosuke Dodo5, Yoshitaka Shirasaki6, Takashi Kamatani7, Akiko Takahashi1,8*
著者の所属機関
1. 公益財団法人がん研究会 がん研究所 細胞老化研究部
2. 京都大学 大学院医学研究科附属 がん免疫総合研究センター
3. 九州大学 大学院工学研究院 機械工学部門
4. 東京薬科大学 生命科学部 生命医科学科 免疫制御学研究室
5. 理化学研究所 環境資源科学研究センター 触媒・融合研究グループ
6. 東京大学 先端科学技術研究センター 光量子イメージング分野
7. 東京科学大学 総合研究院 M&Dデータ科学センター AI技術開発分野
8. 公益財団法人がん研究会 NEXT-Gankenプログラム がん細胞社会成因解明プロジェクト
4.研究の詳細
背景と経緯
細胞老化は、加齢や肥満、放射線・抗がん剤療法などのさまざまなストレスによって誘導され、細胞増殖を停止させるがん抑制機構の一つとして知られています。一方で、老化した細胞(老化細胞)では、炎症性因子を高発現して分泌することから、がんを含むさまざまな加齢関連疾患の発症を促進することが明らかになっており、近年では老化細胞がこれらの疾患の新たな治療標的として注目されています。しかし、老化細胞は正常な細胞に比べて死ににくいゾンビ細胞として知られています。
これまでに、老化細胞では鉄代謝に異常が生じ、細胞内に多量の鉄を蓄積することや、老化細胞に蓄積した鉄が加齢性疾患の発症に関与することが明らかになりつつあります。細胞内で遊離状態の2価鉄イオン(Fe2+)が蓄積すると、脂質過酸化反応が促進され、鉄依存性の細胞死であるフェロトーシスが誘導されることが知られていますが、老化細胞は鉄を蓄積するにもかかわらずフェロトーシスに対して抵抗性を示します。近年、フェロトーシスはがん治療の新たな戦略として注目されており、老化細胞におけるフェロトーシス抵抗性のメカニズムは治療標的となりうると考えられますが、その詳細は不明でした。
研究内容
本研究グループは、老化細胞においてフェロトーシスの原因となる2価鉄イオン(Fe2+)や脂質ラジカル(脂質過酸化反応の過程で生成される物質)が細胞内のリソソームに集中していたことから、リソソームに注目した解析を行った結果、老化細胞におけるリソソームの機能不全がフェロトーシス抵抗性の鍵となっていることを見出しました。通常、リソソームの内部は酸性(pH約4.5)に保たれており、鉄の細胞内分配をはじめとするさまざまな生理機能にこの酸性環境が重要な役割を果たしています。老化細胞では、リソソーム内部が中性に近くなり、その結果として2価鉄イオン(Fe2+)がリソソーム内に閉じ込められることで、2価鉄イオン(Fe2+)によって生じる脂質過酸化反応がリソソーム内に集中し、細胞全体に広がりにくくなるためにフェロトーシスに対する抵抗性を獲得することが示唆されました。さらに、老化細胞ではリソソームを酸性に保つV-ATPaseというタンパク質複合体を構成する一部のタンパク質の量が減少しているために、V-ATPaseの機能が低下していることが、リソソームの酸性度の低下の原因となっていることも明らかになりました。
そこで、V-ATPaseを活性化させる化合物であるEN6を使用し、老化細胞のリソソームを再び酸性化することで、老化細胞のフェロトーシス感受性が回復するか検討しました。その結果、EN6を処置した老化細胞では、リソソーム内に局在していた2価鉄イオン(Fe2+)や脂質ラジカルがリソソーム外に放出され、老化細胞のフェロトーシス感受性が回復しました(図)。また、リソソーム酸性度の低下を伴うフェロトーシス抵抗性は、老化細胞だけでなく、抗がん剤の処置により生じた治療抵抗性のがん細胞においても見られることや、これらのがん細胞にEN6を処置することでリソソームを酸性化した場合も、フェロトーシス感受性が回復することが分かりました。さらに、膵臓がんのモデルマウスにEN6を投与すると、腫瘍組織にフェロトーシスが生じ、がん細胞や老化した間質細胞※6が減少して腫瘍の成長が抑制されるとともに、抗腫瘍免疫※7に関わる免疫細胞(T細胞)が増加することが確認されました(図)。
これらの結果は、老化細胞におけるリソソーム機能不全とフェロトーシス抵抗性との関係を明らかにしたという点に加え、がんを含む加齢性疾患の治療において、老化細胞や治療抵抗性がん細胞におけるリソソーム酸性度を調節することで、疾患の発症や進行を抑制できる可能性を示す点で、画期的な発見です。
5.本研究への支援
本研究は、以下の支援を受けて実施されました。
・国立研究開発法人科学技術振興機構(JST)ムーンショット「細胞内サイバネティック・アバターの遠隔制御によって見守られる社会の実現(プロジェクトマネージャー:山西陽子)」
・国立研究開発法人科学技術振興機構(JST)ムーンショット「生体内ネットワークの理解による難治性がん克服に向けた挑戦(プロジェクトマネージャー:大野茂男)」
・国立研究開発法人科学技術振興機構(JST)共創の場形成支援プログラム(COI-NEXT)「レジリエント健康長寿社会の実現を先導するグローバルエコシステム形成拠点(研究代表者:一木隆範)」
・国立研究開発法人日本医療研究開発機構(AMED)革新的先端研究開発支援事業(AMED- CREST)「細胞老化の根本的原理の理解に基づいた革新的診断・治療戦略の開発(研究代表者:高橋暁子)」
・日本学術振興会(JSPS)科学研究費補助金 挑戦的研究(開拓)「 がん微小環境におけるポリアミン代謝機能解明への挑戦(研究代表者:高橋 暁子)」
・日本学術振興会(JSPS)科学研究費補助金 基盤研究(C)「 老化間質細胞を標的とした新規がん治療法の探索(研究代表者:羅 智文)」
・日本学術振興会(JSPS)科学研究費補助金 基盤研究(C)「 老化細胞から分泌されるエクソソームのがん病態における役割の解明(研究代表者:田中 陽子)」
・日本学術振興会(JSPS)科学研究費補助金 基盤研究(C)「 細胞老化におけるミトコンドリアDNA損傷応答(研究代表者:山内 翔太)」
・日本学術振興会(JSPS)科学研究費補助金 若手研究「老化CAFsにおける翻訳制御を介したSASP誘導およびがん促進機構の解明(研究代表者:菅原 祥)」
・日本学術振興会(JSPS)科学研究費補助金 若手研究「がん組織内の老化血管内皮細胞によるがん悪性化機構の解明(研究代表者:周 翔宇)」
・公益財団法人 武田科学振興財団
・公益財団法人 アステラス病態代謝研究会
6.用語解説
(※1)老化細胞
正常な細胞がDNA損傷などのさまざまなストレスを受けることで生じる、細胞分裂を不可逆的に停止した細胞。増殖性を失っているものの生存を維持し続け、炎症性因子などを分泌することで、がんや動脈硬化、糖尿病、神経変性疾患などの加齢性疾患の発症や進展を促進する。
(※2)フェロトーシス
鉄に依存して細胞内の脂質が酸化されることで生じる過酸化脂質が蓄積することにより引き起こされる、細胞死の形態の一つ。がんの治療抵抗性や神経変性疾患の病態に関わることから、治療標的として注目されている。
(※3)リソソーム
細胞小器官の一つであり、主に細胞内の不要物などの分解を担う。リソソームの内部は酸性に保たれており、酸性環境において高い活性をもつ多くの加水分解酵素が存在する。また、鉄の細胞内輸送や分配においても重要な役割を果たす。
(※4)V-ATPase(vacuolar-type ATPase)
ATPの加水分解によるエネルギーを用いてプロトン(H+)をリソソーム内に輸送し、リソソーム内部を酸性化させる働きをもつプロトン輸送体。リソソーム膜上に存在し、多数のサブユニットから構成される複合体である。
(※5)脂質過酸化反応
細胞内の多価不飽和脂肪酸をはじめとする脂質が活性酸素などにより脂質ラジカルとなり、その後連鎖的に反応して過酸化脂質を生成する過程。生成物によって細胞膜やDNA、タンパク質などが損傷を受け、過度に反応が生じた際はフェロトーシスにつながる。
(※6)がん間質細胞
がん組織を構成するがん細胞以外の細胞のこと。線維芽細胞や内皮細胞、免疫細胞などからなる。がん細胞と密接に相互作用しながら、がん細胞の増殖や浸潤、転移に対して状況によってさまざまな影響を与えることが知られている。
(※7)抗腫瘍免疫
免疫系ががん細胞を異物として認識して攻撃・排除する仕組みのこと。主に細胞傷害性T細胞や
ナチュラルキラー細胞が関与し、がん細胞が発現する異常な分子(がん抗原)によって活性化される。抗腫瘍免疫を活性化することによりがんを治療する「がん免疫療法」が注目されている。
関連PDF
- プレスリリース文書
 (663.9KB )
(663.9KB )