研究内容目次
遺伝子発現解析を基盤とした分子標的治療のゲノミクス研究
標的とする分子を明確にし、その機能を特異的に制御する薬剤 (分子標的薬剤) の探索・開発研究が、抗がん剤開発において中心的な役割を担っています。分子標的薬の臨床導入が進むにつれ、その有効性が明らかになり、また比較的軽微な副作用などから、分子標的薬への期待はますます大きなものとなっています。一方で、分子標的薬は効くか効かないかがはっきりしているという特徴があるため、有効な薬剤を投与するために薬剤反応性を事前に予測するバイオマーカーの開発が大変重要です。 また、効果の期待できないがんに対しては、新たな分子標的の同定が切望されています。
私たちは、マイクロアレイによる遺伝子発現解析技術を活用し、分子標的薬剤の開発に有用なデータベースの構築とそれを用いたバイオマーカー・分子標的の探索研究を進めています。具体的には、分子標的薬剤を含む多くの抗がん化合物をがん細胞に処理し、その結果引き起こされるがん細胞の応答に興味を持ち、網羅的遺伝子発現解析を行っています。これにより、化合物の制がん効果と関連する遺伝子発現変動のデータベースを構築しています。また、研究1)と関連しますが、同様に様々な代謝ストレスをがん細胞に処理し、代謝ストレスによる遺伝子発現変動のデータベースを構築しています。これらの遺伝子発現変動データベースの拡充を進めるとともに、バイオインフォマティクスを活用し、さらには外部のデータベースも援用して、「薬剤反応性予測に有用なバイオマーカー」や「新しい分子標的」の探索研究を行っています。また、遺伝子発現情報の新しい解析技術や遺伝子発現の簡便な測定技術などの開発に取り組んでいます。これらの研究を通じ、分子標的薬開発サイクルの推進に貢献していきたいと考えています。
体系的・網羅的ゲノム解析による分子標的薬開発の革新
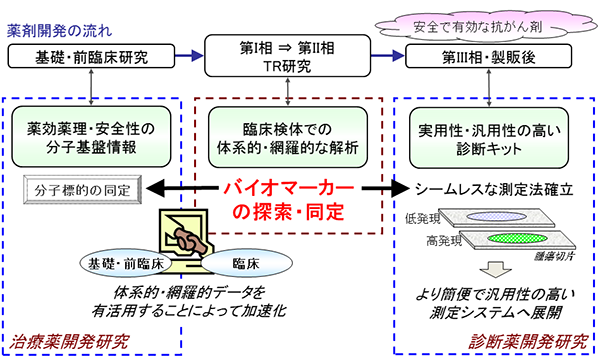
新規の薬剤開発においては、標的の同定や化合物の探索などの基礎研究にはじまり、候補化合物の物性や毒性の評価などの前臨床試験を経て、ヒトでの有効性を評価する臨床試験(I, II, III相、製販後試験)が行われる。薬剤の有効性を診断するバイオマーカーの同定は、比較的早期の臨床試験(I, II相)で行い、その後、バイオマーカーとしての有用性を後期の臨床試験(III相、製販後)で評価するという流れが理想的と考えられている。このように治療薬開発研究と診断薬開発研究を連携して推進することにより、分子標的薬剤の開発サイクルが加速されるものと期待される。