研究内容
- ヒトがん細胞パネル(JFCR39)を用いた薬剤感受性―マルチオミックス統合データベース(JFCR39-DB)の開発と抗がん剤スクリーニング
- 新規PI3K阻害剤ZSTK474の同定と創薬研究
- ゴルジ体を標的とした新規抗がん物質の同定と抗がん分子機序の解析
3. ゴルジ体を標的とした新規抗がん物質の同定と抗がん分子機序の解析
ゴルジ体は、DNAに刻まれた遺伝情報が転写・翻訳されて合成された新生タンパク質が、プロセシングや糖鎖修飾を受け、細胞膜上や細胞外に輸送される過程を制御している。ゴルジ体機能を阻害するブレフェルジン A(BFA)はがん細胞の増殖を抑制するが、医薬品化されていない(1)。分子薬理部ではこれまでに、JFCR39システムを利用して、天然のカビ由来の半合成化合物であるM-COPA(2-メチルコプロフィリンアミド[AMF-26])がBFAと類似したフィンガープリントを示すことから、その作用メカニズムはBFAと同様にゴルジ体の小胞輸送に重要な低分子量GTPアーゼArf1の活性化(GTP結合型)を阻害することによりゴルジ体機能を阻害することに起因すると予測した。そこで、実験的にM-COPAがGTP結合型Arf1を減少させること、ゴルジ体構造を破壊することを示し、本剤が新規ゴルジ体機能阻害剤であることを明らかにした(2)。本剤は元来、トリコデルマ(子嚢菌)由来の天然化合物を原料としており、大量合成が困難であったが、共同研究者の東京理科大学・椎名勇教授が本剤の人工合成に成功し、人工M-COPAが天然由来のものと同等のゴルジ阻害活性、抗がん作用を示すことを明らかにした(3)。そこで、東京理科大学、北里大学、エーザイ株式会社と共同で、科学技術振興機構(JST)(現在は日本医療研究開発機構AMED)の研究成果最適展開支援プログラム(A-STEP)に採用され、創薬研究を進めている。
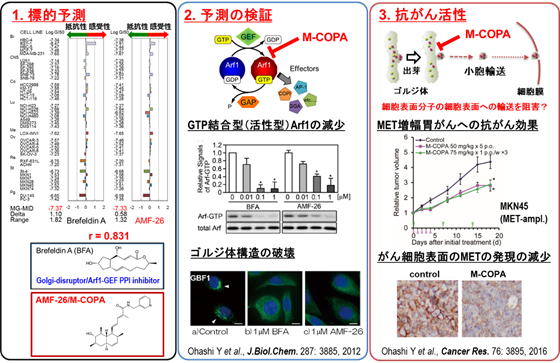
M-COPAは、ゴルジ体機能を阻害するが、ゴルジ体機能阻害がどのような分子機序で抗がん作用を発揮するかはまだ分かっていなかった。分子薬理部では、さまざまながん由来の細胞株について、in vitroおよび動物レベルでM-COPAが奏功するか否かを調べ、本剤が受容体チロシンキナーゼ遺伝子の1つであるMETを増幅している胃がん細胞に奏功することを明らかにした。METはゴルジ体においてプロセッシングを受け、細胞表面まで運搬されるが、M-COPAを曝露することによりin vitroおよび動物レベルでMETのプロセッシングが阻害され細胞表面におけるMETの発現抑制し、MET下流のシグナル伝達を抑制すること、それに伴いがん増殖を抑制することを明らかにした(4)。同様な活性は、FGFR2を過剰発現する胃がん細胞株でも認められた。現在、他の受容体チロシンキナーゼが活性化したがん、チロシンキナーゼ阻害剤(TKI)に耐性を獲得したがんへのM-COPAの抗がん効果を調べており、TKIとは異なる新たな抗がん分子機構を持つ注目の薬剤として研究を進めている。
関連リンク
- 【プレスリリース】新しい作用メカニズムを有する「新規抗がん剤」の人工合成について
- 東京理科大学椎名研究室・がん研究会分子薬理部 合同記者会見 ゴルジ体を標的とする新しい抗がん剤の人工合成に成功
- (英語版)Total Synthesis of AMF-26 (M-COPA), an Antitumor Agent for Inhibition of the Golgi System
- 注目すべき論文「胃がんの新規抗がん物質を同定―ゴルジ体を標的とした新しい治療法開発へ道−」
- (アニメーション入り一般向け解説版)ゴルジ体を標的とする新しい抗がん剤の作用メカニズム 東京理科大学椎名研究室・がん研究会分子薬理部 記者説明会
- (英語版)M-COPA, a Golgi Disruptor, Exhibits Antitumor Activity against MET-Addicted Gastric Cancers
- ダイジェスト版 胃がんの新規抗がん物質M-COPAを同定 −ゴルジ体を標的とした新しい治療法へ道−東京理科大学椎名研究室・がん研究会分子薬理部 記者説明会
参考文献
- Sausville EA, Duncan KL, Senderowicz A, Plowman J, Randazzo PA, Kahn R, Malspeis L, Grever MR. Antiproliferative effect in vitro and antitumor activity in vivo of brefeldin A. Cancer J Sci Am. 1996 Jan-Feb;2(1):52-8.
- Ohashi Y, Iijima H, Yamaotsu N, Yamazaki K, Sato S, Okamura M, Sugimoto K, Dan S, Hirono S, Yamori T. AMF-26, a novel inhibitor of the Golgi system, targeting ADP-ribosylation factor 1 (Arf1) with potential for cancer therapy. J Biol Chem. 2012 Feb 3;287(6):3885-97.
- Shiina I, Umezaki Y, Ohashi Y, Yamazaki Y, Dan S, Yamori T. Total synthesis of AMF-26, an antitumor agent for inhibition of the Golgi system, targeting ADP-ribosylation factor 1. J Med Chem. 2013 Jan 10;56(1):150-9.
- Ohashi Y, Okamura M, Hirosawa A, Tamaki N, Akatsuka A, Wu KM, Choi HW, Yoshimatsu K, Shiina I, Yamori T, Dan S. M-COPA, a Golgi Disruptor, Inhibits Cell Surface Expression of MET Protein and Exhibits Antitumor Activity against MET-Addicted Gastric Cancers. Cancer Res. 2016 Jul 1;76(13):3895-903.