�y�j���[�X�����[�X�z�A���c�n�C�}�[�a�̃A�~���C�h�a���Ɋ֘A���ĕϓ����� �G�N�\�\�[���^���p�N���J�e�v�V��B��]�Ґ��t�ƌ��t���甭�� �`�A���c�n�C�}�[�a�̐V�K�����f�f�@�A���Ö�J���Ɍq����肪����`
2023�N12��11��
�y���\�̃|�C���g�z
�E�A���c�n�C�}�[�a�������N�����a�ԕω��O��̔]�Ґ��t���W�߁A���̒��Ɋ܂܂��זE�O���E�i�G�N�\�\�[���j�̃^���p�N����ԗ��I�ɕ��͂����B
�E�J�e�v�V��B���܂�11��ނ̃G�N�\�\�[���ܗL�^���p�N�����A���c�n�C�}�[�a�̐i�s�ő������邱�Ƃ������B
�E�]�Ґ��t�݂̂Ȃ炸���t���̃G�N�\�\�[���Ɋ܂܂��J�e�v�V��B�͔]�A�~���C�hβ�ʂƑ��ւ��Ă����B
�E�G�N�\�\�[�����J�e�v�V��B�̓A���c�n�C�}�[�a�̐V���ȑ����f�f�o�C�I�}�[�J�[�⎡�Ẫ^�[�Q�b�g�Ƃ��Ċ��҂����B
�y���\�ҁz
���ƌ��������ϑg���A����Ղ̖�a�@�@�F�m�ljȁA�t���L�O���l�a�������@�䌅�V�� (�����ӔC�ҁj
�k�C����w��w�@��[�����Ȋw�����@�@�����@�\����������@���R�k��
�k�C����w��w�@��[�����Ȋw�����@�@�����@�\����������@���d
�������v���V�W����������Z���^�[�@�A�c�K�k
�������v���V�W������Ì����Z���^�[�@���䗝��
���{�ԏ\���Ō��w�@�Ō�w���i�����������j�@�팩�@��
�y���\�̗v�|�z
���ƌ��������ϑg���A����Ղ̖�a�@�@�F�m�ljȁ@�䌅�V���A�k�C����w��w�@��[�����Ȋw�����@�@�����@�\����������@���R�k���A�������v���V�W������Ì����Z���^�[�@�A�c�K�k��𒆐S�Ƃ��錤���O���[�v�́A�A���c�n�C�}�[�a�i���P�j�a�Ԃ�������O��̔팱�҂̔]�Ґ��t�i���Q�j����G�N�\�\�[���i���R�j�𒊏o���A�����Ɋ܂܂��^���p�N����ԗ��I�ɕ��͂��܂����B���̌��ʁA�A���c�n�C�}�[�a�̐i�s�ߒ��ŗʓI�ɕϓ�����11��ނ̃G�N�\�\�[���ܗL�^���p�N�������肳��A�Ȃ��ł��J�e�v�V��B�͔]�Ґ��t�̃A�~���C�hβ�ʂƑ��ւ��Ă��܂����B
�F�m�ǂ̖�U�����߂�A���c�n�C�}�[�a�́A���ǂ�10�N�ȏ�O����a�C�̌����ƂȂ�]�̕a�ς��n�܂邱�Ƃ��m���Ă��܂��B�a�ς̐i�s���x��ATN���ށi�A�~���C�hβ�a��[A]�A�^�E�^���p�N���a��[T]�A�_�o�ϐ�[N]�j�ƌĂ�镪�ޖ@�i��4�j�ɂ���ċ敪����܂��B����̌����ł͂܂��A�A���c�n�C�}�[�a�A�y�x�F�m�@�\��Q�iMCI�j�A����҂���]�Ґ��t�J�ɍ̎�E���W��ATN���ނ��s���܂����B����ɃA���c�n�C�}�[�a�̕a���ω����m���Ȕ팱�҂ƑS������Ȕ팱�҂ɍi�荞�݂܂����B�����Ĕ]�Ґ��t����G�N�\�\�[����P�����A�G�N�\�\�[���Ɋ܂܂��^���p�N���𐢊E�ō����x�̎��ʕ��͑��u�Ŗԗ��I�ɒ�ʕ��͂��܂����B���̌��ʁA�G�N�\�\�[������1,756��ނ̃^���p�N�������肳��A���̒��ňقȂ�ATN���ރX�e�[�W�ԁi�A���c�n�C�}�[�a�̕a�����i�s����ߒ��j�ŗʓI�ɕϓ�����^���p�N����11��ޔ�������܂����B
������ƃA�~���C�hβ�a�����̊Ԃŕϓ����������G�N�\�\�[���^���p�N���̈�ł���J�e�v�V��B�i��5�j�́A136��̑�K�͌��؎����Ŕ]�Ґ��t�݂̂Ȃ炸�A���t���̃G�N�\�\�[���ɂ����Ă����l�̕ϓ����m�F����܂����B�G�N�\�\�[���͔]�����̏�킩�錌�t�o�C�I�}�[�J�[�Ƃ��Ă̗��p�����҂���Ă���A����̔����̓A���c�n�C�}�[�a�̐V���Ȑf�f�p�o�C�I�}�[�J�[�J���̎肪����ƂȂ�\��������܂��B�����ɂ����̃G�N�\�\�[���^���p�N���̕ω��̓A���c�n�C�}�[�a�̕a���`���̃��J�j�Y���Ɋ֗^����\��������A���Â̕W�I���Ƃ��Ă������̐i�W�����҂���܂��B
�Ȃ��A�{�������ʂ́A���{����2023�N12��11���i���j���J�̈�w���wBrain�x�I�����C���łɌf�ڂ����\��ł��B
�y�����̔w�i�z
�����J���Ȃɂ��܂��ƁA���{�̔F�m�ǂ̊��҂�2020�N�̎��_��600���l�Ɛ��v����2025�N�ɂ͂��悻700���l�ɂ̂ڂ�Ɨ\������Ă��܂��B�A���c�n�C�}�[�a�i�ȉ��uAD�v�Ƃ����B�j�́A�F�m�ǂ̌����ƂȂ�a�C�̈�œ��{�ł͔F�m�ǂƐf�f���ꂽ����҂�6���ȏ���߂Ă��܂��BAD�ǂ����l�̔]�ł́A�u�A�~���C�hβ�i�ȉ��uAβ�v�Ƃ����B�j�v��u�����_���^�E�i�ȉ��up-Tau�v�Ƃ����B�j�v�ƌĂ��ُ�ȃ^���p�N�������܂��Ă���A����ɂ��_�o�זE�����A�]���ޏk���A�]�̓������ቺ����ƍl�����Ă��܂��B
AD���ǂ̖�25�N�O����Aβ���]�ɒ~�ς��J�n����Ɣ]�Ґ��t�i�ȉ��uCSF�v�Ƃ����B�j����Aβ42�i���U)�͌������A��10�N�O����CSF����p-Tau���������܂��B�₪�Ċ������~�N���O���A���_�o���ǂ������N������A�̐_�o�ϐ��̉ߒ��̓A�~���C�h�J�X�P�[�h�����ƌĂ�A���݂̕a�ԏC����J���̎嗬�ɂȂ��Ă��܂��B�܂��G�N�\�\�[������Đ_�o�זE�Ԃł����̕a�����^���p�N�����g�U���A�a�C���i�s����ƌ����Ă��܂��B
����AAD�a�ԏC����̊J�������Ƃ��ɑ����f�f��ڎw�����g�݂�������2018�N�A�č��̍����V���������ƃA���c�n�C�}�[����iNIA-AA�j�̓o�C�I�}�[�J�[�ɂ��AD�̕a���w�I�Ȑi�s�ߒ��ނ����K�C�h���C���ł���ATN���ށi��4�j���J�����A�Տ��f�f���琶���w�I�f�f�ւ̈ڍs���܂����B���ꂩ��q���g����X�́AATN���ނ�P�Ȃ镪�ނł͂Ȃ��A���� ➡ Aβ�~�� ➡��-Tau�~��/�_�o�ϐ��̂��ꂼ��̕ω��Ő�����ŗL�̃^���p�N������ԑŐs�ɑ����邱�Ƃ��ł���c�[���ƍl���܂����B�������ACSF�̎�E�ۑ��̉ߒ��ł�Aβ�Ȃǂ̋z�����₷���^���p�N���͔��Ɏ����₷���A�̎�҂�{�݊Ԃő���덷�������邱�Ƃ����ɂȂ��Ă��܂��B�����ŁA�P��{�݂̈�l�̈�t���A�^���p�N�����z�����ɂ������ŌJ��Ԃ����t���̎悵�A���t�Ɋ܂܂��^���p�N���̕ϐ��Ƌz���ɂ��r����h���܂����B����ɍ̎悩��Ȃ�ׂ����������ۑ����邽�߁A�Ղ̖�a�@�Տ��������̃V�X�e���𗘗p�����̂̕i���Ǘ����s���܂����B�����̌��̂�p���A�G�N�\�\�[����Ώۂɂ����V�����a���^���p�N���ƃo�C�I�}�[�J�[���̒T�����s���܂����B�Ȃ��A���̌����͌Ղ̖�a�@�Տ������ϗ��ψ���ɏ��F����i�Տ������ԍ�1388�j�q�g��ΏۂƂ�����Â���ь��N�����ϗ��K�C�h���C���ɏ������Ď��{����܂����B
�y������@�Ɛ��ʁz
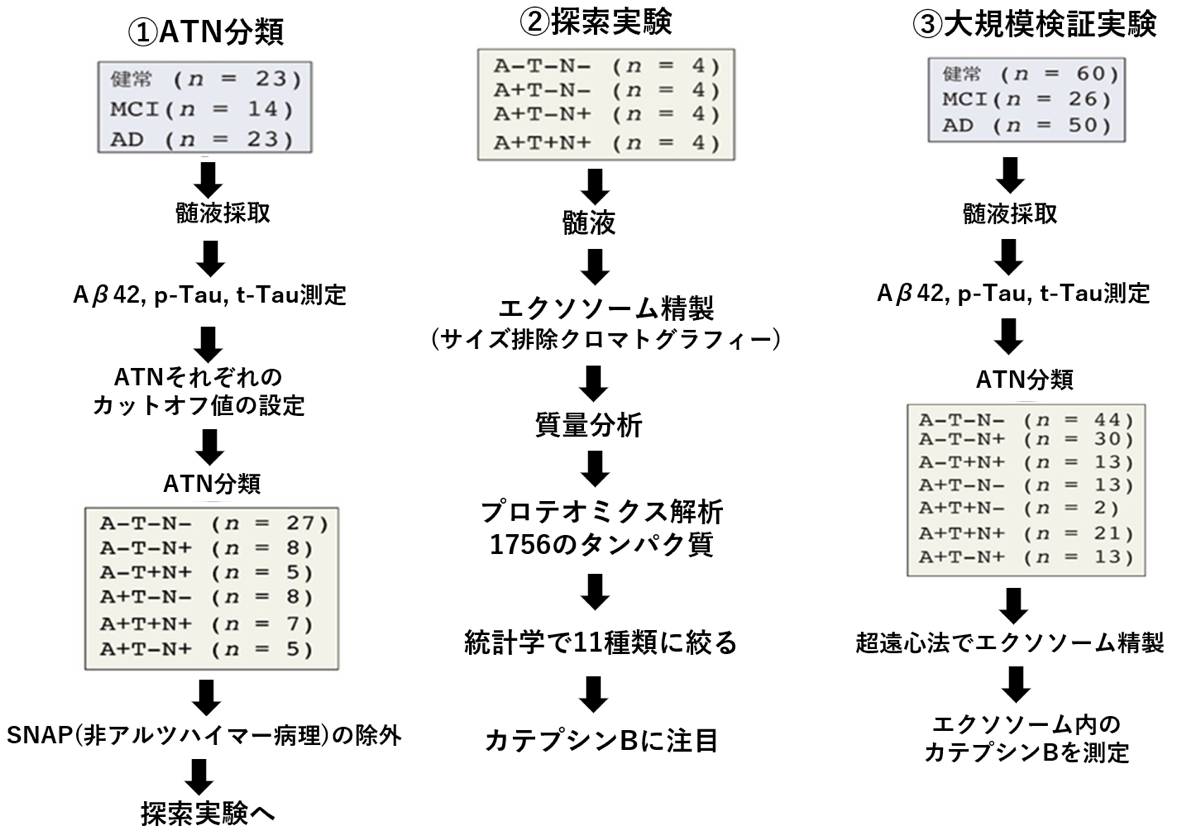
���̌�����2017�N�S������2021�N�S���ɌՂ̖�a�@�̔F�m�ljȊO���ōs���A136�l�̓��{�l���ҁi�j��71�l�A����65�l�A���ϔN��71.3�j�����ӂ���ɎQ�����܂����BAD����50�l�AMCI����26�l�A����ѐ���ΏƎ�60�l�ł����B�̎�E�ۑ����ꂽCSF���̂�Aβ42�A��-Tau�A���^�E�it-Tau�j�𑪒肵�AATN���ނ��s���܂����B����SNAP�Q�i���V�j�����S�ɏ��O���AAD�o�C�I�}�[�J�[�l������Ȋ��҂Ə�����AD���҂݂̂�I�����i�A�T�������j�A�����̕a���w�I�i�s�Ɗ֘A�����A�̃G�N�\�\�[���^���p�N���肷�邽�߂�CSF �G�N�\�\�[���̃v���e�I�~�N�X�v���t�@�C�����O�i���W�j�����{���܂��� �i�}1�j�B
CSF���琸�����ꂽ�G�N�\�\�[���́AOrbitrap Fusion Lumos���ʕ��͑��u�iThermo Scientific�Ёj���g�p���ĕ��͂���A1,756��ނ̃^���p�N�������o����܂����B���̒����琳��➡Aβ�~��➡��-Tau�~��/�_�o�ϐ��ƕa���ω����i�s����ߒ��ŁA���̗ʂ��ω�����11��ނ̃^���p�N����������܂��� (�}2)�B
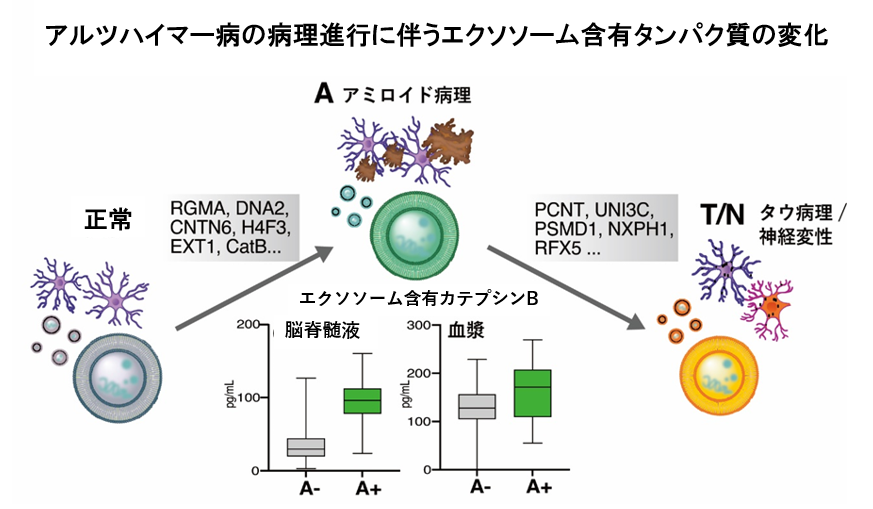
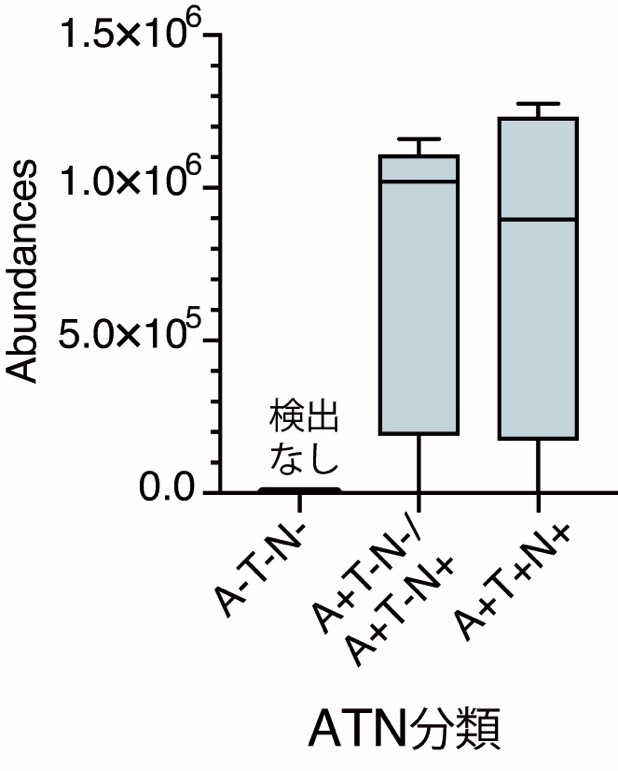
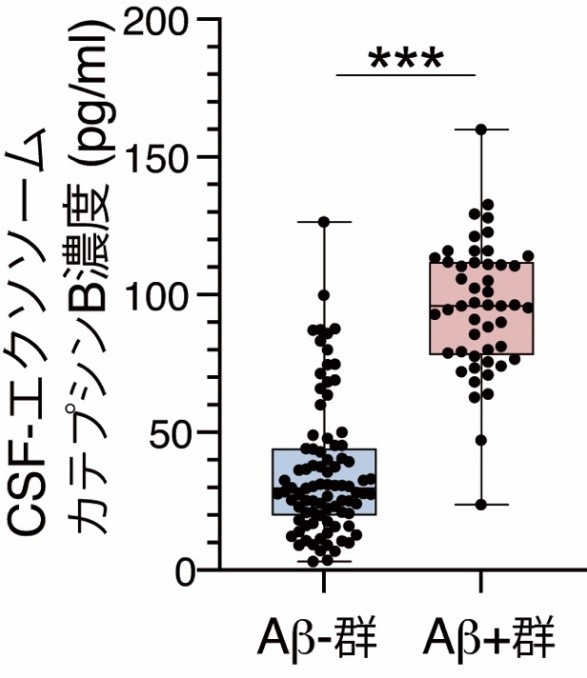
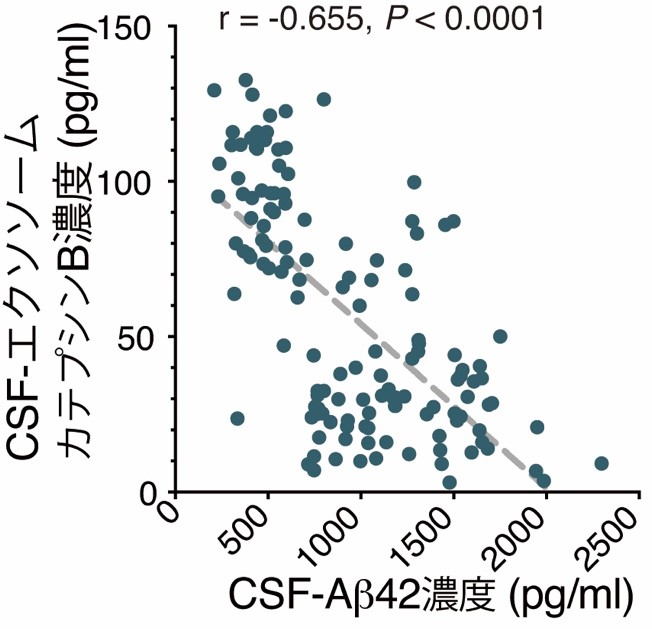
�����̃^���p�N���̂����J�e�v�V��B�́A��K�͌��؎����ɂ����Ă�CSF����ь��t���̃G�N�\�\�[���œ��v�w�I�ɗL�ӂȗʓI�ϓ����m�F����܂����B��̓I�ɂ́AATN���ނɂ�����A-T-N-����A+T-N±�ɕω������CSF�G�N�\�\�[���ܗL�J�e�v�V��B���������Ă��܂����i�}�R�j�B Aβ�A���iA-�j�Ɣ�r����Aβ�z���iA+�j�ł�CSF�G�N�\�\�[���ܗL�J�e�v�V��B�ʂ��������i�}�S�j�ACSF-Aβ42�ʁi�A�~���C�h�a���̎w�W�j�Ƒ��ւ��Ă��܂����i�}�T�j�B
�����̃^���p�N����AD�̕a���Ɋ֗^���邾���łȂ��A�����ȃA���c�n�C�}�[�a���҂���肷�邽�߂̐V���ȃo�C�I�}�[�J�[���Ǝ��Ẫ^�[�Q�b�g�Ƃ��ė��p�ł���\��������܂��B���肳�ꂽ11��̃^���p�N���̒��ɂ��܂܂Œm���Ă��Ȃ������A���c�n�C�}�[�a�̔��ǂ̌������B��Ă���\��������܂��B�Ƃ��ɃJ�e�v�V��B�̓A���c�n�C�}�[�a�̑����a���̃A�~���C�h�`���i�K����ւ���Ă���Ƃ�����������A�J�e�v�V��B�̓�����W�����̒��ɂ̓A�~���C�hβ�̎Y����ቺ��������̂�����܂��B�����G�N�\�\�[���J�e�v�V��B�̌v���ɂ���Ĕ]��Aβ�~�ς𑁊��Ɍ��o�ł���\��������A��ƂƋ��͂����t���̃G�N�\�\�[���J�e�v�V��B���ȕցA�����Ɍ��o�ł��鑁���A���c�n�C�}�[�a�f�f�L�b�g�̊J�������Ă��܂��B
�y�����_���^�C�g���z
Extracellular Vesicle Proteome Unveils Cathepsin B Connection to Alzheimer’s Disease Pathogenesis.
�y���Җ��zKohei Yuyama, Hui Sun, Risa Fujii, Isao Hemmi, Koji Ueda and Yukifusa Igeta*
�y�f�ڎ����zBrain
�y�o�ŎЖ��zOxford University Press.
�y�c�n�h�z10.1093/brain/awad361.
�y�ӎ��z
�{�����ɂ����͒����܂����A��������̊��҂���Ƃ��̂��Ƒ��ɐS���犴�Ӑ\���グ�܂��B
�y�p�����z
�i���P�j�A���c�n�C�}�[�a�͐i�s���̐_�o�ϐ������ŁA�L����Q�┻�f�͂̒ቺ����Ǐ�ł��B�]���ɃA�~���C�h�^���p�N���ƃ����_���^�E�^���p�N�����~�ς��A�_�o�זE�����N�����܂��B�y�x�̋L����Q����n�܂�A�i�K�I�ɍ����]�@�\��Q���i�s���܂��B�a�ԏC���Ö@���J������A�R�A�~���C�h�Ö@�ł��郌�J�l�}�u���{�M�ŏ��߂ĕی����F�ɂȂ�܂����B
�i���Q�j�]�Ґ��t�͔]���������F�����ȉt�̂ŃA���c�n�C�}�[�a�Ȃǔ]�����̌����^���p�N�����r������Ă��܂��B�F�m�ǂ̐f�f�ɑ����̗L�v�ȃ^���p�N�����������炵�܂��B
�i���R�j�G�N�\�\�[���͂�����זE���番�傳��钼�a���\�i�m���[�g���T�C�Y�̍זE�O���E�̈��ŕ��匳�זE�̃^���p�N���A�����A�j�_���܂܂�܂��B���t�ȂǑ̉t����G�N�\�\�[������ĕa���זE�̕��q�������o����f�f�@�̓��L�b�h�o�C�I�v�V�[�i�̉t�����j�Ƃ������A���t����]�זE�̂��܂��܃^���p�N�����`�q�̏��ɃA�N�Z�X�����i�Ƃ��ďd�v�ł��B
�i���S�jATN���ނ́A�A���c�n�C�}�[�a�̏Ǐ�͍l���ɓ��ꂸ�A�a���̐i�s�i�K��]������V�X�e���ł��BA-T-N-�i���ׂẴo�C�I�}�[�J�[������j�AA+T-N-�i�A�~���C�h�̂ݗz���j�Ȃǂƕ\������܂��B�Տ��f�f���ꂽ�A���c�n�C�}�[�^�F�m�ǂ̖�30���́ASNAP �isuspected non-Alzheimer's disease pathophysiology �j�ƌĂ��A���c�n�C�}�[�a�ł͂Ȃ������iA-T+N±�AA-T-N+�j���܂܂�܂��BATN���ނł͂���SNAP���������Ƃ��ł��A���팒��҂Ə����ȃA���c�n�C�}�[�a���҂ɍi�荞�ނ��Ƃ��ł��܂��B
�i���T�j�J�e�v�V��B�iCathepsin B�j�́A��Ƀ��\�\�[���Ƃ����זE���̏��튯�ɑ��݂���^���p�N�������y�f�ł��B���������^���p�N���̕����A�y�f�����̒��߁A�זE�����̐���Ɋ֗^���A���ǐ�������_�o�ϐ������A����ȂǂƂ̊֘A����������Ă��܂��B�A�~���C�h�J�X�P�[�h�����ł́AA�̓A�~���C�h�O��̃^���p�N���iAPP�j���琶������܂����A����ɂ�����APP�ؒf�y�f1�iBACE1�j��γ-�Z�N���^�[�[�Ƃ����y�f���֗^����ƌ����Ă���܂��B�������J�e�v�V��B��A�̐����Ɋ֗^����β�Z�N���^�[�[�ł���Ƃ̕�����A�J�e�v�V���a�j�Q��̓��^���`�q�j�Q�ŃA���c�n�C�}�[�a���җR���̔|�{�זE��}�E�X���f����A����A����уA�~���C�h���������������A�L����Q�����P�������ƕ���Ă��܂��B
�i���U�jA42�Ƃ̓A�~���C�h�^���p�N���̈��42�̃A�~�m�_���琬��y�v�`�h�ł��B�A���c�n�C�}�[�a�̕a���w�I�ȍŏ����̕a�ςł���Ɠ����ɁA�Q�d���̂�R�d���̂��`�����A���ڐ_�o�זE�ɓŐ��������ƌ����Ă��܂��B
�i���V�jSNAP�isuspected non-Alzheimer's disease pathophysiology�j�́A�Տ��f�f�ł̓A���c�n�C�}�[�^�F�m�ǂƐf�f���ꂽ�Ǘ�̒��ŁA��AD�a�����^����P�[�X�̂��Ƃł��B���̌o�߂̓A���c�n�C�}�[�^�F�m�ǂ��x���A���퐶���ɑ傫�Ȏx����������܂���B�w�i�����͑��l�ŁAA�̕ω����Ȃ��^�E�ُ݈̂�𗈂��^�E�I�p�`�[���܂܂�܂��B
�i���W�j�v���e�I�~�N�X�v���t�@�C�����O�Ƃ́A���̓��^���p�N���̑�K�͂ȕ��͂̂��Ƃł��B�v���e�I�~�N�X��͂̓^���p�N���̓���A��ʉ�́A�|���C���̌����Ɏg�p�����d�v�ȋZ�p�ł��B�v���t�@�C�����O�Ƃ́A����̑�������������ڍׂȏ��邽�߂ɍs����v���Z�X���w���܂��B����̌����ł́A�t�̃N���}�g�O���t�B�[���ʕ��͑��u�iLC/MS�j�ƌĂ��@����g�p���v���e�I�~�N�X��͂��s���܂����B
�E�A���c�n�C�}�[�a�������N�����a�ԕω��O��̔]�Ґ��t���W�߁A���̒��Ɋ܂܂��זE�O���E�i�G�N�\�\�[���j�̃^���p�N����ԗ��I�ɕ��͂����B
�E�J�e�v�V��B���܂�11��ނ̃G�N�\�\�[���ܗL�^���p�N�����A���c�n�C�}�[�a�̐i�s�ő������邱�Ƃ������B
�E�]�Ґ��t�݂̂Ȃ炸���t���̃G�N�\�\�[���Ɋ܂܂��J�e�v�V��B�͔]�A�~���C�hβ�ʂƑ��ւ��Ă����B
�E�G�N�\�\�[�����J�e�v�V��B�̓A���c�n�C�}�[�a�̐V���ȑ����f�f�o�C�I�}�[�J�[�⎡�Ẫ^�[�Q�b�g�Ƃ��Ċ��҂����B
�y���\�ҁz
���ƌ��������ϑg���A����Ղ̖�a�@�@�F�m�ljȁA�t���L�O���l�a�������@�䌅�V�� (�����ӔC�ҁj
�k�C����w��w�@��[�����Ȋw�����@�@�����@�\����������@���R�k��
�k�C����w��w�@��[�����Ȋw�����@�@�����@�\����������@���d
�������v���V�W����������Z���^�[�@�A�c�K�k
�������v���V�W������Ì����Z���^�[�@���䗝��
���{�ԏ\���Ō��w�@�Ō�w���i�����������j�@�팩�@��
�y���\�̗v�|�z
���ƌ��������ϑg���A����Ղ̖�a�@�@�F�m�ljȁ@�䌅�V���A�k�C����w��w�@��[�����Ȋw�����@�@�����@�\����������@���R�k���A�������v���V�W������Ì����Z���^�[�@�A�c�K�k��𒆐S�Ƃ��錤���O���[�v�́A�A���c�n�C�}�[�a�i���P�j�a�Ԃ�������O��̔팱�҂̔]�Ґ��t�i���Q�j����G�N�\�\�[���i���R�j�𒊏o���A�����Ɋ܂܂��^���p�N����ԗ��I�ɕ��͂��܂����B���̌��ʁA�A���c�n�C�}�[�a�̐i�s�ߒ��ŗʓI�ɕϓ�����11��ނ̃G�N�\�\�[���ܗL�^���p�N�������肳��A�Ȃ��ł��J�e�v�V��B�͔]�Ґ��t�̃A�~���C�hβ�ʂƑ��ւ��Ă��܂����B
�F�m�ǂ̖�U�����߂�A���c�n�C�}�[�a�́A���ǂ�10�N�ȏ�O����a�C�̌����ƂȂ�]�̕a�ς��n�܂邱�Ƃ��m���Ă��܂��B�a�ς̐i�s���x��ATN���ށi�A�~���C�hβ�a��[A]�A�^�E�^���p�N���a��[T]�A�_�o�ϐ�[N]�j�ƌĂ�镪�ޖ@�i��4�j�ɂ���ċ敪����܂��B����̌����ł͂܂��A�A���c�n�C�}�[�a�A�y�x�F�m�@�\��Q�iMCI�j�A����҂���]�Ґ��t�J�ɍ̎�E���W��ATN���ނ��s���܂����B����ɃA���c�n�C�}�[�a�̕a���ω����m���Ȕ팱�҂ƑS������Ȕ팱�҂ɍi�荞�݂܂����B�����Ĕ]�Ґ��t����G�N�\�\�[����P�����A�G�N�\�\�[���Ɋ܂܂��^���p�N���𐢊E�ō����x�̎��ʕ��͑��u�Ŗԗ��I�ɒ�ʕ��͂��܂����B���̌��ʁA�G�N�\�\�[������1,756��ނ̃^���p�N�������肳��A���̒��ňقȂ�ATN���ރX�e�[�W�ԁi�A���c�n�C�}�[�a�̕a�����i�s����ߒ��j�ŗʓI�ɕϓ�����^���p�N����11��ޔ�������܂����B
������ƃA�~���C�hβ�a�����̊Ԃŕϓ����������G�N�\�\�[���^���p�N���̈�ł���J�e�v�V��B�i��5�j�́A136��̑�K�͌��؎����Ŕ]�Ґ��t�݂̂Ȃ炸�A���t���̃G�N�\�\�[���ɂ����Ă����l�̕ϓ����m�F����܂����B�G�N�\�\�[���͔]�����̏�킩�錌�t�o�C�I�}�[�J�[�Ƃ��Ă̗��p�����҂���Ă���A����̔����̓A���c�n�C�}�[�a�̐V���Ȑf�f�p�o�C�I�}�[�J�[�J���̎肪����ƂȂ�\��������܂��B�����ɂ����̃G�N�\�\�[���^���p�N���̕ω��̓A���c�n�C�}�[�a�̕a���`���̃��J�j�Y���Ɋ֗^����\��������A���Â̕W�I���Ƃ��Ă������̐i�W�����҂���܂��B
�Ȃ��A�{�������ʂ́A���{����2023�N12��11���i���j���J�̈�w���wBrain�x�I�����C���łɌf�ڂ����\��ł��B
�y�����̔w�i�z
�����J���Ȃɂ��܂��ƁA���{�̔F�m�ǂ̊��҂�2020�N�̎��_��600���l�Ɛ��v����2025�N�ɂ͂��悻700���l�ɂ̂ڂ�Ɨ\������Ă��܂��B�A���c�n�C�}�[�a�i�ȉ��uAD�v�Ƃ����B�j�́A�F�m�ǂ̌����ƂȂ�a�C�̈�œ��{�ł͔F�m�ǂƐf�f���ꂽ����҂�6���ȏ���߂Ă��܂��BAD�ǂ����l�̔]�ł́A�u�A�~���C�hβ�i�ȉ��uAβ�v�Ƃ����B�j�v��u�����_���^�E�i�ȉ��up-Tau�v�Ƃ����B�j�v�ƌĂ��ُ�ȃ^���p�N�������܂��Ă���A����ɂ��_�o�זE�����A�]���ޏk���A�]�̓������ቺ����ƍl�����Ă��܂��B
AD���ǂ̖�25�N�O����Aβ���]�ɒ~�ς��J�n����Ɣ]�Ґ��t�i�ȉ��uCSF�v�Ƃ����B�j����Aβ42�i���U)�͌������A��10�N�O����CSF����p-Tau���������܂��B�₪�Ċ������~�N���O���A���_�o���ǂ������N������A�̐_�o�ϐ��̉ߒ��̓A�~���C�h�J�X�P�[�h�����ƌĂ�A���݂̕a�ԏC����J���̎嗬�ɂȂ��Ă��܂��B�܂��G�N�\�\�[������Đ_�o�זE�Ԃł����̕a�����^���p�N�����g�U���A�a�C���i�s����ƌ����Ă��܂��B
����AAD�a�ԏC����̊J�������Ƃ��ɑ����f�f��ڎw�����g�݂�������2018�N�A�č��̍����V���������ƃA���c�n�C�}�[����iNIA-AA�j�̓o�C�I�}�[�J�[�ɂ��AD�̕a���w�I�Ȑi�s�ߒ��ނ����K�C�h���C���ł���ATN���ށi��4�j���J�����A�Տ��f�f���琶���w�I�f�f�ւ̈ڍs���܂����B���ꂩ��q���g����X�́AATN���ނ�P�Ȃ镪�ނł͂Ȃ��A���� ➡ Aβ�~�� ➡��-Tau�~��/�_�o�ϐ��̂��ꂼ��̕ω��Ő�����ŗL�̃^���p�N������ԑŐs�ɑ����邱�Ƃ��ł���c�[���ƍl���܂����B�������ACSF�̎�E�ۑ��̉ߒ��ł�Aβ�Ȃǂ̋z�����₷���^���p�N���͔��Ɏ����₷���A�̎�҂�{�݊Ԃő���덷�������邱�Ƃ����ɂȂ��Ă��܂��B�����ŁA�P��{�݂̈�l�̈�t���A�^���p�N�����z�����ɂ������ŌJ��Ԃ����t���̎悵�A���t�Ɋ܂܂��^���p�N���̕ϐ��Ƌz���ɂ��r����h���܂����B����ɍ̎悩��Ȃ�ׂ����������ۑ����邽�߁A�Ղ̖�a�@�Տ��������̃V�X�e���𗘗p�����̂̕i���Ǘ����s���܂����B�����̌��̂�p���A�G�N�\�\�[����Ώۂɂ����V�����a���^���p�N���ƃo�C�I�}�[�J�[���̒T�����s���܂����B�Ȃ��A���̌����͌Ղ̖�a�@�Տ������ϗ��ψ���ɏ��F����i�Տ������ԍ�1388�j�q�g��ΏۂƂ�����Â���ь��N�����ϗ��K�C�h���C���ɏ������Ď��{����܂����B
�y������@�Ɛ��ʁz
���̌�����2017�N�S������2021�N�S���ɌՂ̖�a�@�̔F�m�ljȊO���ōs���A136�l�̓��{�l���ҁi�j��71�l�A����65�l�A���ϔN��71.3�j�����ӂ���ɎQ�����܂����BAD����50�l�AMCI����26�l�A����ѐ���ΏƎ�60�l�ł����B�̎�E�ۑ����ꂽCSF���̂�Aβ42�A��-Tau�A���^�E�it-Tau�j�𑪒肵�AATN���ނ��s���܂����B����SNAP�Q�i���V�j�����S�ɏ��O���AAD�o�C�I�}�[�J�[�l������Ȋ��҂Ə�����AD���҂݂̂�I�����i�A�T�������j�A�����̕a���w�I�i�s�Ɗ֘A�����A�̃G�N�\�\�[���^���p�N���肷�邽�߂�CSF �G�N�\�\�[���̃v���e�I�~�N�X�v���t�@�C�����O�i���W�j�����{���܂��� �i�}1�j�B

�}�P�@����̎����̗���
CSF���琸�����ꂽ�G�N�\�\�[���́AOrbitrap Fusion Lumos���ʕ��͑��u�iThermo Scientific�Ёj���g�p���ĕ��͂���A1,756��ނ̃^���p�N�������o����܂����B���̒����琳��➡Aβ�~��➡��-Tau�~��/�_�o�ϐ��ƕa���ω����i�s����ߒ��ŁA���̗ʂ��ω�����11��ނ̃^���p�N����������܂��� (�}2)�B

�}�Q�@�A���c�n�C�}�[�a�̕a���i�s�ɔ����G�N�\�\�[���ܗL�^���p�N���̕ω�
�����̃^���p�N���̂����J�e�v�V��B�́A��K�͌��؎����ɂ����Ă�CSF����ь��t���̃G�N�\�\�[���œ��v�w�I�ɗL�ӂȗʓI�ϓ����m�F����܂����B��̓I�ɂ́AATN���ނɂ�����A-T-N-����A+T-N±�ɕω������CSF�G�N�\�\�[���ܗL�J�e�v�V��B���������Ă��܂����i�}�R�j�B Aβ�A���iA-�j�Ɣ�r����Aβ�z���iA+�j�ł�CSF�G�N�\�\�[���ܗL�J�e�v�V��B�ʂ��������i�}�S�j�ACSF-Aβ42�ʁi�A�~���C�h�a���̎w�W�j�Ƒ��ւ��Ă��܂����i�}�T�j�B

�}�R A-T-N-����A+T-N±�ւ̕ω���CSF�G�N�\�\�[���ܗL�J�e�v�V��B������

�}�S A�A���iA-�j�Q�Ɣ�r����A�z���iA+�j�Q�ł�CSF�G�N�\�\�[���ܗL�J�e�v�V��B�ʂ�����

�}�T�@CSF�G�N�\�\�[���ܗL�J�e�v�V��B��CSF A42�ƕ��̑��ւɂ���
�����̃^���p�N����AD�̕a���Ɋ֗^���邾���łȂ��A�����ȃA���c�n�C�}�[�a���҂���肷�邽�߂̐V���ȃo�C�I�}�[�J�[���Ǝ��Ẫ^�[�Q�b�g�Ƃ��ė��p�ł���\��������܂��B���肳�ꂽ11��̃^���p�N���̒��ɂ��܂܂Œm���Ă��Ȃ������A���c�n�C�}�[�a�̔��ǂ̌������B��Ă���\��������܂��B�Ƃ��ɃJ�e�v�V��B�̓A���c�n�C�}�[�a�̑����a���̃A�~���C�h�`���i�K����ւ���Ă���Ƃ�����������A�J�e�v�V��B�̓�����W�����̒��ɂ̓A�~���C�hβ�̎Y����ቺ��������̂�����܂��B�����G�N�\�\�[���J�e�v�V��B�̌v���ɂ���Ĕ]��Aβ�~�ς𑁊��Ɍ��o�ł���\��������A��ƂƋ��͂����t���̃G�N�\�\�[���J�e�v�V��B���ȕցA�����Ɍ��o�ł��鑁���A���c�n�C�}�[�a�f�f�L�b�g�̊J�������Ă��܂��B
�y�����_���^�C�g���z
Extracellular Vesicle Proteome Unveils Cathepsin B Connection to Alzheimer’s Disease Pathogenesis.
�y���Җ��zKohei Yuyama, Hui Sun, Risa Fujii, Isao Hemmi, Koji Ueda and Yukifusa Igeta*
�y�f�ڎ����zBrain
�y�o�ŎЖ��zOxford University Press.
�y�c�n�h�z10.1093/brain/awad361.
�y�ӎ��z
�{�����ɂ����͒����܂����A��������̊��҂���Ƃ��̂��Ƒ��ɐS���犴�Ӑ\���グ�܂��B
�y�p�����z
�i���P�j�A���c�n�C�}�[�a�͐i�s���̐_�o�ϐ������ŁA�L����Q�┻�f�͂̒ቺ����Ǐ�ł��B�]���ɃA�~���C�h�^���p�N���ƃ����_���^�E�^���p�N�����~�ς��A�_�o�זE�����N�����܂��B�y�x�̋L����Q����n�܂�A�i�K�I�ɍ����]�@�\��Q���i�s���܂��B�a�ԏC���Ö@���J������A�R�A�~���C�h�Ö@�ł��郌�J�l�}�u���{�M�ŏ��߂ĕی����F�ɂȂ�܂����B
�i���Q�j�]�Ґ��t�͔]���������F�����ȉt�̂ŃA���c�n�C�}�[�a�Ȃǔ]�����̌����^���p�N�����r������Ă��܂��B�F�m�ǂ̐f�f�ɑ����̗L�v�ȃ^���p�N�����������炵�܂��B
�i���R�j�G�N�\�\�[���͂�����זE���番�傳��钼�a���\�i�m���[�g���T�C�Y�̍זE�O���E�̈��ŕ��匳�זE�̃^���p�N���A�����A�j�_���܂܂�܂��B���t�ȂǑ̉t����G�N�\�\�[������ĕa���זE�̕��q�������o����f�f�@�̓��L�b�h�o�C�I�v�V�[�i�̉t�����j�Ƃ������A���t����]�זE�̂��܂��܃^���p�N�����`�q�̏��ɃA�N�Z�X�����i�Ƃ��ďd�v�ł��B
�i���S�jATN���ނ́A�A���c�n�C�}�[�a�̏Ǐ�͍l���ɓ��ꂸ�A�a���̐i�s�i�K��]������V�X�e���ł��BA-T-N-�i���ׂẴo�C�I�}�[�J�[������j�AA+T-N-�i�A�~���C�h�̂ݗz���j�Ȃǂƕ\������܂��B�Տ��f�f���ꂽ�A���c�n�C�}�[�^�F�m�ǂ̖�30���́ASNAP �isuspected non-Alzheimer's disease pathophysiology �j�ƌĂ��A���c�n�C�}�[�a�ł͂Ȃ������iA-T+N±�AA-T-N+�j���܂܂�܂��BATN���ނł͂���SNAP���������Ƃ��ł��A���팒��҂Ə����ȃA���c�n�C�}�[�a���҂ɍi�荞�ނ��Ƃ��ł��܂��B
�i���T�j�J�e�v�V��B�iCathepsin B�j�́A��Ƀ��\�\�[���Ƃ����זE���̏��튯�ɑ��݂���^���p�N�������y�f�ł��B���������^���p�N���̕����A�y�f�����̒��߁A�זE�����̐���Ɋ֗^���A���ǐ�������_�o�ϐ������A����ȂǂƂ̊֘A����������Ă��܂��B�A�~���C�h�J�X�P�[�h�����ł́AA�̓A�~���C�h�O��̃^���p�N���iAPP�j���琶������܂����A����ɂ�����APP�ؒf�y�f1�iBACE1�j��γ-�Z�N���^�[�[�Ƃ����y�f���֗^����ƌ����Ă���܂��B�������J�e�v�V��B��A�̐����Ɋ֗^����β�Z�N���^�[�[�ł���Ƃ̕�����A�J�e�v�V���a�j�Q��̓��^���`�q�j�Q�ŃA���c�n�C�}�[�a���җR���̔|�{�זE��}�E�X���f����A����A����уA�~���C�h���������������A�L����Q�����P�������ƕ���Ă��܂��B
�i���U�jA42�Ƃ̓A�~���C�h�^���p�N���̈��42�̃A�~�m�_���琬��y�v�`�h�ł��B�A���c�n�C�}�[�a�̕a���w�I�ȍŏ����̕a�ςł���Ɠ����ɁA�Q�d���̂�R�d���̂��`�����A���ڐ_�o�זE�ɓŐ��������ƌ����Ă��܂��B
�i���V�jSNAP�isuspected non-Alzheimer's disease pathophysiology�j�́A�Տ��f�f�ł̓A���c�n�C�}�[�^�F�m�ǂƐf�f���ꂽ�Ǘ�̒��ŁA��AD�a�����^����P�[�X�̂��Ƃł��B���̌o�߂̓A���c�n�C�}�[�^�F�m�ǂ��x���A���퐶���ɑ傫�Ȏx����������܂���B�w�i�����͑��l�ŁAA�̕ω����Ȃ��^�E�ُ݈̂�𗈂��^�E�I�p�`�[���܂܂�܂��B
�i���W�j�v���e�I�~�N�X�v���t�@�C�����O�Ƃ́A���̓��^���p�N���̑�K�͂ȕ��͂̂��Ƃł��B�v���e�I�~�N�X��͂̓^���p�N���̓���A��ʉ�́A�|���C���̌����Ɏg�p�����d�v�ȋZ�p�ł��B�v���t�@�C�����O�Ƃ́A����̑�������������ڍׂȏ��邽�߂ɍs����v���Z�X���w���܂��B����̌����ł́A�t�̃N���}�g�O���t�B�[���ʕ��͑��u�iLC/MS�j�ƌĂ��@����g�p���v���e�I�~�N�X��͂��s���܂����B
�֘APDF
- �j���[�X�����[�X����
 (1,938.5KB )
(1,938.5KB )