目次
- がん分子標的薬耐性機構の解明と耐性克服薬の探索
- がん幹細胞(Cancer stem cell)の機能解析と分子標的の同定
- 生存増殖シグナル伝達系の解析と分子標的の探索
- がん免疫療法への耐性機構の解明と克服法の探索
- 血小板との相互作用を介したがん悪性化機構の解明とそれに基づく創薬
- 骨肉腫・脳腫瘍に対する新規治療標的と治療法候補の探索
がん幹細胞(Cancer stem cell)の機能解析と分子標的の同定
がんは日本における死亡原因の第1位であり、その治療法の開発のために多くの取り組みがなされているが、依然として外科的切除が可能な初期のがんを除き、非常に治癒が困難である。
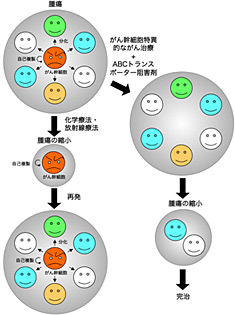 手術不能ながんの多くは化学療法、放射線療法で治療されるが、完全に腫瘍細胞を排除することは極めて難しく、多くの場合、治療抵抗性細胞が出現し、再発してしまうことが大きな問題である。再発・転移の原因として近年提唱されているのが、がん幹細胞仮説である。がん幹細胞仮説は、腫瘍組織中にも、正常組織と同様な幹細胞が存在し、それらは自己を複製する能力を持つとともに、少数存在するだけで元の腫瘍組織と同様の腫瘍を形成する能力をもつことが示されてきている。さらに、がん幹細胞は抗がん剤や放射線への抵抗性を有しているため治療の際に残存しやすく、再発・転移の原因となっていると考えられている。したがって、がん幹細胞を標的とした治療法を確立することで再発、転移のリスクの少ないがん治療へとつながることが期待される。そのためには、がん幹細胞の性状を理解することが重要であるが、その存在比率が低く、また現在のところがん幹細胞のみを分離する方法がないため、がん幹細胞の性状解析は非常に困難である。現在では、正常組織幹細胞の濃縮、分離方法を応用してがん幹細胞研究が進められており、白血病幹細胞の研究においては、がん幹細胞を標的とした治療法の探索・マウスモデルでの治療の段階まで研究が進んでいる。しかし、固形がんにおいては、分離、濃縮方法の確立もまだ不十分であり、がん幹細胞研究はまだまだこれからの研究領域である。そこで当研究部では、がん幹細胞が幹細胞様性質を維持する分子機構、がん幹細胞特異的マーカーの同定、がん幹細胞の分化・細胞死を誘導できるターゲット分子の同定を目標に研究を進めている。
手術不能ながんの多くは化学療法、放射線療法で治療されるが、完全に腫瘍細胞を排除することは極めて難しく、多くの場合、治療抵抗性細胞が出現し、再発してしまうことが大きな問題である。再発・転移の原因として近年提唱されているのが、がん幹細胞仮説である。がん幹細胞仮説は、腫瘍組織中にも、正常組織と同様な幹細胞が存在し、それらは自己を複製する能力を持つとともに、少数存在するだけで元の腫瘍組織と同様の腫瘍を形成する能力をもつことが示されてきている。さらに、がん幹細胞は抗がん剤や放射線への抵抗性を有しているため治療の際に残存しやすく、再発・転移の原因となっていると考えられている。したがって、がん幹細胞を標的とした治療法を確立することで再発、転移のリスクの少ないがん治療へとつながることが期待される。そのためには、がん幹細胞の性状を理解することが重要であるが、その存在比率が低く、また現在のところがん幹細胞のみを分離する方法がないため、がん幹細胞の性状解析は非常に困難である。現在では、正常組織幹細胞の濃縮、分離方法を応用してがん幹細胞研究が進められており、白血病幹細胞の研究においては、がん幹細胞を標的とした治療法の探索・マウスモデルでの治療の段階まで研究が進んでいる。しかし、固形がんにおいては、分離、濃縮方法の確立もまだ不十分であり、がん幹細胞研究はまだまだこれからの研究領域である。そこで当研究部では、がん幹細胞が幹細胞様性質を維持する分子機構、がん幹細胞特異的マーカーの同定、がん幹細胞の分化・細胞死を誘導できるターゲット分子の同定を目標に研究を進めている。
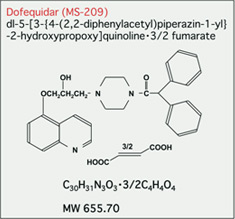
がん化学療法センターではこれまでに、ABCトランスポーターファミリーの阻害剤開発を進めてきた。その過程で、Dofequidarという薬剤ががん幹細胞様細胞における抗がん剤排出を抑制すること(Cancer Sci., 2009)、マイクロアレイを用いて発現解析を行うことで、がん幹細胞様細胞では抗がん剤耐性に関わるある種のmiRNA発現が高いこと(Oncol. Res., 2010)などを見いだしている。これらの研究をさらに進展させていくことで、がん幹細胞で破綻している分子機構を見出し、それを新しい分子標的治療へとつなげていきたいと考えている。最近では、ALK融合遺伝子陽性肺がんにおいて、CrizotinibやCeritinibといった治療薬(ALK阻害薬)に耐性となった症例から、ABCトランスポーターファミリーの1つであるABCB1(P糖たんぱく質)が過剰発現して耐性となっている症例があることなども発見し報告している。
Recent publications:
- P-glycoprotein Mediates Ceritinib Resistance in Anaplastic Lymphoma Kinase-rearranged Non-small Cell Lung Cancer. *Katayama R, Sakashita T, Yanagitani N, Ninomiya H, Horiike A, Friboulet L, Gainor JF, Motoi N, Dobashi A, Sakata S, Tambo Y, Kitazono S, Sato S, Koike S, John Iafrate A, Mino-Kenudson M, Ishikawa Y, Shaw AT, Engelman JA, Takeuchi K, *Nishio M, *Fujita N.
EBioMedicine, 2016 Jan; 3: 54–66. - Transforming growth factor-β decreases the cancer-initiating cell population within diffuse-type gastric carcinoma cells. Ehata S, Johansson E, Katayama R, Koike S, Watanabe A, Hoshino Y, Katsuno Y, Komuro A, Koinuma D, Kano MR, Yashiro M, Hirakawa K, Aburatani H, Fujita N, *Miyazono K. Oncogene, 2011 Apr 7; 30(14): 1693-705.
- AP-1-dependent miR-21 expression contributes to chemoresistance in cancer stem cell-like SP cells.
Misawa A, Katayama R, Koike S, Tomida A, Watanabe T, *Fujita N.
Oncol. Res., 2010;19(1)23-33 - Dofequidar fumarate sensitizes cancer stem-like side population cells to chemotherapeutic drugs by inhibiting ABCG2/BCRP-mediated drug export.
Katayama R, Koike S, Sato S, Sugimoto Y, Tsuruo T, *Fujita N.
Cancer Sci. 2009 Nov;100(11):2060-8.