- HOME
- がんに関する情報
- 治療法について
- 薬物療法(化学療法)
- 疾患別の薬物療法
疾患別の薬物療法
目次
Chapter.1: 乳がんに対する薬物療法
抗がん剤療法の有効性
乳がんに対する抗がん剤療法の有効性は確立されています。しかし、乳がんの置かれた状況によって期待できる抗がん剤療法の効果も異なります。
大きく分けて3つの状況があります。
- 転移・再発乳がんでは症状の緩和と延命が期待できます。
- 手術の前に抗がん剤療法先行する場合(術前化学療法といいます)にはがんの縮小に伴い、温存手術、縮小手術が期待できます。
- 手術後の補助療法では予防的抗がん剤療法により治癒する確率が高くなります。
抗がん剤以外に乳がんの治療には副作用が軽微なホルモン療法という選択があります。抗がん療法の治療効果には限界があり、少なからず副作用を有することから、抗がん剤をいつどのような目的で行うのか、適切な判断をするのが重要です。
転移・再発乳がんの抗がん剤療法
アンソラサイクリンの代表薬剤はアドリアマイシンとエピルビシンです。アドリアマイシンを含むCAF療法(またはFAC療法) またはエピルビシンを含むFEC療法(またはCEF療法)が現在の標準的治療であり、その奏効率は50〜60%です。
チューブリン阻害剤であるタキサンの有効性も確立されています。タキサンにはドセタキセルとパクリタキセルがあります。タキサンの奏効率は30〜50%を期待できます。アンソラサイクリンが効かない場合にもタキサンの効果は期待できます。反対にタキサンが効かない場合にはアンソラサイクリンの効果が期待できます。アンソラサイクリンとタキサンは乳がんの治療の中心となる薬剤と考えられています。
そのほかの抗がん剤には S−1、カペシタビン、エリブリン、ゲムシタビン、ビノレルビンなどがあります。
HER2陽性の乳がんに対してはトラスツズマブの有用性が証明されています。HER2陽性乳がんに対する薬剤には、ペルツズマブ、トラスツズマブ・エムタンシン、ラパチニブなどがあります。
抗がん剤の使用による不快感
抗がん剤で気持ち悪くなったり、食欲が落ちてしまうのはつらいものです。現在は、抗がん剤による吐き気、おう吐を予防する薬が発達してかなりおさえられるようになりました。
アドリアマシンやエピルビシンを含む治療はもっとも吐き気を起こす可能性があります。
アドリアマシンを投与して数時間はなんともないことが多いのですが、投与日の夜や翌日になってから吐き気がでることがしばしばあります。吐き気は普通、 2〜4日間ほど続きますが、その後、徐々に回復し1週間もたてばなんともなくなります。吐き気が1週間以上も長びくのは非常に敏感な方の場合ですがまれなことです。アドリアマイシンは通常3週間に1回の頻度で行う治療ですので、最初の1週間は調子が悪くなりますがそのあとは普通に食欲も戻ります。
従って、延々と気持ち悪い、食べられないわけではありませんので、やせ衰えて体力がなくなってしまうことはまずありません。反対に、がんばって食べ過ぎて太ってしまう方もいらっしゃいます。アドリアマイシン以外の抗がん剤では吐き気はずっと軽く、楽な場合が多いと予想されます。
吐き気はひとによってかなり個人差があります。全くなんともないひともたくさんいます。吐き気があっても軽い人も多いですし、ひどい吐き気を起こす方はむしろ少ないのです。このような個人差をあらかじめ科学的に予測することはまだできません。はじめから吐き気が強いと思いこんで治療を受けないで、病気を良くするチャンスを逃すのはもったいないことです。
抗がん剤の使用による脱毛
ある種の良く効く抗がん剤、例えばアドリアマイシン、エピルビシン、ドセタキセル、パクリタキセルでは頭の髪の毛はほとんど抜けます。抗がん剤を注射してすぐに抜けるわけではありません。通常は投与後、約2週間経ってから抜け始め、3週間目になるとバサバサとぬけます。4〜5週間たつとほとんど抜けてしまいます。
治療をどのくらいの期間、続けるかは病状と副作用の様子によって違ってきますが、通常は数ヶ月続けることが多くなります。従って、治療を続けている間は髪の毛は抜けた状態が続きます。
しかし、治療が終了すれば抗がん剤の影響はとれて、必ず髪の毛は生えてきます。抗がん剤が終了してから3ヶ月たつと短い毛は生えそろい、6ヶ月もするともとの髪の毛に戻ります。残念ながら、脱毛を予防する薬や方法はありません。髪の毛が抜けている間はかつらを利用して頂くのが良いでしょう。
髪の毛が抜けることはショックですが、治療効果を最大限にあげるときは、このような抗がん剤をどうしても使わなければならないことがあります。もしどうしても脱毛が嫌なかたは、髪の毛が抜けにくい他の治療があなたにとって適切な治療かどうか主治医とよく相談してください。
抵抗力の低下
抗がん剤を注射したあと1〜2週後には血液の白血球が低下することが一般的です。
抗がん剤の種類や量にもよりますが、白血球の減少がひどいときに発熱した場合は注意する必要があります。
白血球が少ないとばい菌に対する抵抗力が弱くなり、風邪をひくとすぐに発熱することがあります。高い熱がでたときになにもしないでいると、こじらせて肺炎になってしまうことがあります。肺炎を予防するために、もし熱が37.5℃以上になったときは抗生物質の薬をすぐに飲み始めてください。いったん、飲み始めたら最低3日間は内服を続けて下さい。
そのときのためにあらかじめ抗生物質のお薬を処方しますので、お手元に置いていつでも飲めるようにしておいてください。もし、抗生物質の内服を開始して翌日になっても熱が下がる傾向がないときや、そのほかに心配な症状があるときは、主治医の先生に電話でご連絡ください。ご様子を伺ったうえで、早急に抗生物質の点滴や白血球を上げる注射などを行う必要があるかを判断します。場合によっては入院が必要な場合もあります。
実際に肺炎になってしまうのは珍しいですが、このように、あらかじめ入念な対策をとることで肺炎はほとんど未然に防ぐことができます。風邪をひかないように気をつけていただくことは大事ですが、あまり神経質になる必要もありません。人混みで風邪を拾わないように気をつけることは望ましいことですが、どうしても人混みのなかに出なくてはならないこともあると思います。たとえば、通院のとき混んだ電車に乗ってこなくてはならないとか、自分で買い物をしなくてはならないとか、生活のうえで必要なことは仕方がありません。しかしその際、他人のつばや、せき払いが直接かかることに注意して下さい。
マスクをつけていただくと、つばや、せき払いのような濃厚な感染を防げます。マスクで風邪をすべて防げるわけではありませんが、治療直後から白血球が低下している間の時期(治療のあと1〜2週間まで)に人混みに出るときはマスクをすることをお勧めします。可能ならば、予定を治療の影響のない時期に延期していただいたほうが無難でしょう。
パクリタキセルの副作用について
パクリタキセルではくすりのアレルギーを起こすことがあります。
もし、いままでに他の薬で強いアレルギーを起こしたことのあるかたはパクリタキセルを使用できません。
アレルギーを予防するために、抗がん剤投与の30分前に抗ヒスタミン剤を内服した後、ステロイドと抗セロトニン剤を点滴注射します。実際に強いアレルギー症状をおこすことは極めてまれですが、軽いアレルギー症状はときにあります。パクリタキセルの治療では頭の髪の毛はほとんど抜けてしまいます。
しかし、注射してすぐに抜けるわけではありません。通常は投与後、約2週間経ってから抜け始め4〜5週間たつとほとんど抜けてしまいます。
治療を続けている間は髪の毛は抜けた状態が続きます。しかし、治療が終了すれば抗がん剤の影響はとれて、必ず髪の毛は生えてきます。抗がん剤が終了してから3ヶ月たつと短い毛は生えそろい、6ヶ月もするともとの髪の毛に戻ります。
残念ながら、脱毛を予防する薬や方法はありません。髪の毛が抜けている間はかつらを利用して頂くのも良いでしょう。パクリタキセルの治療で気持ち悪くなることはほとんどありません。軽い吐き気や、食欲低下がみられることがありますが、強いものはないだろうと予測しています。
むしろ、食欲が増えて食べ過ぎてしまうこともあります。念のため、吐き気予防の薬は点滴で使用します。点滴回数が増えるにつれて、手の指先、足の指先にピリピリとしびれを感じることがあります。症状が強いときは治療を休む場合もあります。
ときには、体が疲れやすい、関節痛、筋肉痛、口内炎、味覚の変化、爪の変化、便秘、むくみ、めまい、肝機能異常などがありますが、程度は軽いことがほとんどです。まれな副作用としては血圧低下、不整脈、間質性肺炎が報告されています。
分子標的薬剤としてのトラスツズマブの意義
HER2(ハーツー) (Human Epidermal Growth Factor Receptor Type 2)はヒトがん遺伝子のひとつです。その産物であるタンパク質は膜蛋白質受容体です。
トラスツズマブはHER2受容体に対するモノクローナル抗体です。
HER2過剰発現をした転移乳がんの治療薬、再発予防薬と有用です。
一般的にはHER2存在の有無は簡便な免疫組織法(ハーセプ・テスト)で判定します。3+の陽性の場合またはFISH陽性の場合トラスツズマブは適応となります。全乳がんの約20%がHER2陽性です。治療の効果をあらかじめ正確に予測し、治療計画をたてることは重要です。例えば、ホルモン・レセプター陽性の場合にはホルモン療法の有効性は高いことが予測されますのでホルモン療法が適応となります。
しかし、抗がん剤ではその有効性を確実に予測する方法は未だに確立されていません。抗がん剤は様々な作用機序を有し、単一の標的ではありません。モノクローナル抗体であるトラスツズマブはHER2のみを標的とする薬剤であり、鍵(key)と錠(lock)の関係となります。HER2が存在して始めてトラスツズマブが効く可能性があります。
このようにHER2を検査することにより、治療方針を明確に決定できるようになりました。個人、がんの個性にあった治療が可能となりました。分子標的薬剤は抗がん剤ほど広域ではなく、対象は限られますが標的の有無により治療の選択ができるのが最大の利点です。
トラスツズマブの副作用について
最も現れやすい副作用は発熱です。10人中4-5人の割合で38度以上の発熱が見られます。
この発熱は2-3日以内に落ち着くことがほとんどです。発熱があったときは解熱剤が有効ですので適切に対処します。その他、悪寒(さむけ)全身倦怠感(だるさ)熱感、戦慄(ふるえ)、吐き気、嘔吐、食欲低下、頻脈(どきどき感)、肝障害、などが10人に1-2人の割合で見られます。
その他、骨痛、ほてり、頭痛、筋肉痛、胸部痛、上腕痛、しびれ、咳、目やに、耳鳴りなど報告がありますが頻度は低いものです。いずれの副作用も一時的な症状でおさまると予想されます。まれな副作用として注意しなくてはならないのは心臓への副作用です。通常の状態では現れないと予測されますが、以前に心臓の病気をしたことのある方、アドリアマイシンのような抗がん剤をたくさん受けた方、胸部に放射線治療をたくさん受けた方では注意をして行う必要があります。
もし、心臓の機能が落ちている場合はトラスツズマブが使用できません。安全に治療を行うために、前もって心臓の機能の検査を受けて頂きます。具体的には内科 (循環器)の心臓の専門の先生の診察を受けた後、心臓の超音波検査(エコー)で心臓の機能を調べます。最近、胸部レントゲン撮影、心電図の検査をしていない場合は、内科受診の前にそれらの検査を受けてください。その結果を心臓の先生が見て、超音波検査(エコー)を行います。
その他、ショック、呼吸不全、肝不全、白血球減少、腎障害、昏睡、敗血症などの副作用の報告がありますが、その頻度は稀です。これらは全身状態が極めて悪いときには起こるかもしれませんので、全身の体力、臓器の機能が保たれているときにトラスツズマブの治療を受けるようにお勧めします。体力が十分あるときはまずおこらないと予想しています。狂牛病(伝染性海綿状脳症)がトラスツズマブにより伝播したという報告はありません。トラスツズマブの製造過程で牛のひ臓由来成分を含む培地を使用していますので、可能性が絶対ないとは言い切れません。
しかし、この危険よりも治療を受けて得られる利益のほうがずっと大きいと考えられます。
ホルモン療法の種類
乳がんに対するホルモン療法は、がん細胞への女性ホルモンの影響を何らかの仕組みで抑えるものです。
一般に使用されているホルモン剤は以下のように分類されます。
- LHRH アゴニスト:ゴセデリン酢酸塩、リュープロレリン酢酸塩
- 中枢神経を介して卵巣からの女性ホルモン分泌を減少させ、閉経を人工的に起こします。 抗エストロゲン剤:タモキシフェンクエン酸塩、トレミフェンクエン酸塩、フルベストラント
- 女性ホルモン(エストロゲン)が乳がん細胞に作用して刺激するのを抑えます。 アロマターゼ阻害剤:アナストロゾール、レトロゾール、エキセメスタン
- 閉経後の方で脂肪、がん組織等でエストロゲンが作られるのを抑えます。
- プロゲステロン剤: メドロキシプロゲステロン酢酸エステル
- 女性ホルモンの一種ですが、エストロゲン産生を抑えるなど種々の作用があります。
- *ホルモン治療と併用する最近の分子標的薬剤としては、パルボシクリブ、エベロリムスなどの薬剤があります。
ホルモン療法の副作用について
ホルモン療法は抗がん剤療法に比較すると副作用は軽度で安全ですが、次のような副作用が考えられます。乳がんに対するホルモン療法はほとんどが女性ホルモン(特にエストロゲン)の作用を抑えるものですので、自然に女性ホルモンが減少する更年期と同じような症状が出る可能性があります。とくにのぼせ、顔の紅潮、そして膣(ちつ)分泌物の異常、月経異常が多くなります。
特にLHRH アゴニストは卵巣からの女性ホルモン分泌を減少させ、更年期と全く同じような症状を起こす可能性があります。また抗エストロゲン剤、アロマターゼ阻害剤、プロゲステロン剤も同じような症状をおこします。例えばタモキシフェンクエン酸塩の臨床試験では強いのぼせ・顔の紅潮が約17%、膣分泌物の異常が約8%、偽薬より多かったと報告されています。
なお、うつ状態、うつ病についてはホルモン療法による明かな増加は報告されていません。強い吐き気を伴うことはまずありませんが、アロマターゼ阻害剤では時に吐き気のために薬を飲み続けられない方がいらっしゃいます。プロゲステロン剤は食欲亢進、肥満をしばしば来たし、抗がん剤による食欲低下やがん悪液質 (進行がんによる痩せ、体力低下)の治療薬として使われるほどです。
タモキシフェンクエン酸塩も食欲亢進、肥満を来すと考えられていますが、偽薬との比較では差がなかったとされています。プロゲステロン剤は血糖上昇、血圧上昇を来すことがあり、糖尿病、高血圧症の方は注意が必要です。タモキシフェンクエン酸塩は血中コレステロールを10%程度低下させる良い作用がありますが、凝固機能(血液を固まらせる働き)を亢進させる作用もあります。心筋梗塞、脳梗塞、静脈血栓症の病気の方は注意が必要ですので主治医と良くご相談ください。
タモキシフェンクエン酸塩は子宮内膜にたいしては刺激的に働きますので、子宮体がんの発生を約2.5倍に増やすことが知られています。しかし日本女性の子宮体がんの発生率は一万人に2人程度なので、それほど大きい危険ではないと考えています。
念のためにタモキシフェンクエン酸塩服用時は定期的に婦人科検診を受けられることをお薦めします。
当院では婦人科での半年毎の検診をお願いしています。また、月経の異常、異常な膣からの出血があれば婦人科を受診してください。
他のホルモン剤では今のところ二次性のがんの発生は報告されていません。女性ホルモン(エストロゲン)は骨を保護する働きがあるので、LHRHアゴニスト、アロマターゼ阻害剤は骨粗鬆(そしょう)症(骨が薄くなる病気)を発症・進行させる可能性があり、現在どのような薬によってこれを予防できるかが検討されています。タモキシフェンクエン酸塩は骨に対しては保護的に働き、骨粗鬆症の進行を抑えるのではないかと考えられています。
その他の副作用としてタモキシフェンクエン酸塩による網膜症、白内障が報告されています。
術前抗がん剤療法
乳がん手術の前に抗がん剤療法を先行する場合を術前化学療法(術前抗がん剤療法)といいます。
術前抗がん剤療法の意義は次の3点です。
- 術前抗がん剤療法により乳房温存の可能性が高くなります。
- 術前抗がん剤療法の効果をみることにより、予後の予測を行うことができ、術後の治療方針を最適なものに選択できます。
- 抗がん剤療法を術前に行っても、術後に使用する場合に比較して治癒率や生存期間が劣ることはありません。
一般的にはがんの大きさが大きい局所進行乳がんにおいては術前抗がん剤療法が標準治療となっています。
手術後のがんの状態について
手術によって明らかな「がん」は取り除かれます。
ただし、手術では取りきれない、肉眼では見えないがん細胞がまだ残っている可能性があります。それらのがん細胞は通常の検査をしても見つけることはできません。顕微鏡でも分かるか分からないかぐらいのわずかなものです。
また、わずかながん細胞でも時間が経つと再発となって現れます。再発を抑えて乳がんが治る確率をできるかぎり上げるためには予防治療が必要です。手術だけで高率に治ってしまう場合には強い抗がん剤治療は必要ありませんが、ある程度以上の再発の危険がある場合にはしっかりとした再発予防治療が必要です。
治療が必要となるもっとも重要な指標(目安)は乳がん周囲のリンパ節へのがん転移の個数です。手術のとき周囲のリンパ節は取り除かれますが、それらのリンパ節の1個にでも乳がん細胞が存在した場合には抗がん剤治療が必要です。
一般にがん細胞が見つかったリンパ節の数が多いほど再発の危険が増します。また、リンパ節に転移がなかった場合でもその他に、がん細胞の顔つきが悪いとき、がんがリンパ管のなかに入っているときなど、再発の危険が予想される場合は抗がん剤治療を行うこともあります。
ごくわずかな微小ながん細胞を根絶するには全身的な薬による治療が適しています。抗がん剤またはホルモン剤は血流に乗って全身にいきわたり、その効果を発揮するからです。
再発予防のための抗がん剤の必要性
乳がんに対する抗がん剤療法の有効性は確立されています。しかし、乳がんの置かれた状況によって期待できる抗がん剤療法の効果も異なります。
大きく分けて3つの状況があります。
- 転移・再発乳がんでは症状の緩和と延命が期待できます。
- 手術の前に抗がん剤療法先行する場合(術前化学療法といいます)にはがんの縮小に伴い、温存手術、縮小手術が期待できます。
- 手術後の補助療法では予防的抗がん剤療法により治癒する確率が高くなります。
抗がん剤以外に乳がんの治療には副作用が軽微なホルモン療法という選択があります。抗がん療法の治療効果には限界があり、少なからず副作用を有することから、抗がん剤をいつどのような目的で行うのか、適切な判断をするのが重要です。
再発予防に使用される抗がん剤
治療の中心となる抗がん剤はアドリアマイシン(A)またはエピルビシン(E)です。アドリアマイシン(またはエピルビシン)に加えて、他の抗がん剤、シクロホスファミド(C)・フルオロウラシル(F)を同時に行う併用抗がん剤療法が標準的方法のひとつ英語の頭文字をとってCAF療法またはFAC療法またはFEC療法またはCEF療法と言います。フルオロウラシルを含まないAC療法, EC療法もあります。また、腋窩リンパ節転移が陽性の場合はタキサンを追加することによりさらに再発を減らすことができます。AC療法4サイクルの治療後にパクリタキセル週1回を毎週12回またはドセタキセル3週毎4回を行います。
脱毛をおこす原因の抗がん剤はアドリアマイシン(またはエピルビシン)です。しかし、この薬は治療効果を挙げるうえでもっとも重要です。アドリアマイシン (またはエピルビシン)を含まない治療方法も従来から行われていますが、それらの治療方法に比べてアドリアマイシン(またはエピルビシン)を含む治療法の効果は10年生存率で5%優れることが分かっています。
2人に1人の方には閉経前の方では卵巣機能を低下させ生理を止める作用があり、長く続く場合もあります。これらの副作用は確かに無視できるものではありませんが、それ以上に抗がん剤療法による治癒率が改善することが証明されています。抗がん剤を行うことにより再発を半分近く減少させることが証明されています。
稀な副作用としては1,000人に1-2人の割合で抗がん剤によって白血病などの別のがんができることがあります。
もし乳がんが再発した場合、その後に抗がん剤療法を受けてもかなり効果はありますが、最終的にがんを治しきるのは大変難しくなります。抗がん剤を後にとっておこうと思わないで、より早い段階で抗がん剤を十分に使い、治しきると言う目的に力を注いだほうが良いと考えます。
従って、手術直後に十分に抗がん剤治療受けられることをお勧めします。
5%の改善とは少ないようにも思えますが、1,000人のうち50人の命が助かるという数字です。従って、一般にはアドリアマイシン(またはエピルビシン)を含む治療を選択することをお勧めします。なお、アドリアマイシン(またはエピルビシン)には心臓への影響がありますが、予定している薬の量は安全な範囲内のものです。心臓の検査をして安全を確認してから開始します。
再発予防のためのホルモン治療
ホルモン療法を行う必要のある場合は、ホルモン・レセプター(エストロゲン・レセプターまたはプロゲステロン・レセプター)が陽性の場合です。ホルモン剤はがん細胞のホルモン・レセプターと結合してがんの増殖を抑えます。
ホルモン・レセプターは手術で取り除いたがん細胞で検査します。ホルモン療法は副作用が少なく、安全な方法です。ホルモン療法は再発を半分近く減少させます。タモキシフェンは5〜10年間毎日内服します。
閉経前で生理がある場合はゴセレリン酢酸塩またはリュープロレリン酢酸塩を4週間に1回皮下注射し、2〜5年間続けます。閉経後の方はアロマターゼ阻害剤であるアナストロゾール、レトロゾール、エキセメスタンが有効です。アナストロゾール、レトロゾールを5年間内服します。タモキシフェンクエン酸塩を2-3年または5年内服後アロマターゼ阻害剤に変更して継続する治療方法も有用です。
これらのホルモン療法では脱毛もなく、吐き気もありませんが、更年期症状と似た、ほてり、紅潮、のぼせ、めまい、発汗などの症状が一時的にでることがあります。
長期的な副作用としてはタモキシフェンクエン酸塩によって子宮内膜がんが発生の危険が増えますがその頻度は1,000人のうち1-2人と稀な現象ですので、タモキシフェンクエン酸塩の利益のほうが遙かに大きいのです。アロマターゼ阻害剤は骨密度が低下し骨そしょう症の傾向になることがあります。1年に1回骨密度の検査をすることをお勧めします。
Chapter.2: 血液腫瘍に対する薬物療法
リンパ腫について
リンパ組織は、リンパ節とそれを結ぶ細い管(リンパ管)よりなりますが、扁桃腺、胸腺、脾臓なども含まれ、全身に分布しています。リンパ組織はリンパ球を中心に免疫をつかさどり、感染やがんに対する防御機能の中心的な役割を果たしています。
リンパ腫はこのリンパ組織から発生する悪性腫瘍です。リンパ腫は、国際的な病型分類であるWHO分類に基づいて診断・分類されています。WHO分類では、がん化したリンパ球の成熟段階によって「前駆型」(幼弱な若い段階でのがん化)と「成熟型」(成熟した段階でのがん化)に分けられます。前駆型は、リンパ芽球性白血病/リンパ腫としてそれぞれB細胞性、T細胞性、NK細胞性に分けられます。前駆型は急性リンパ性白血病と一連の疾患として扱われます。成熟型はホジキンリンパ腫、B細胞リンパ腫、T/NK細胞リンパ腫に大別され、いわゆる「リンパ腫」とは成熟型を指します。このうち、B細胞リンパ腫が全体の70%強と最も頻度が高く、次いでT/NK細胞リンパ腫が20%弱、ホジキンリンパ腫は10%弱の発症頻度です。
リンパ腫の症状
リンパ腫の多くは、首の周りや縦隔(両方の肺の間)、腋窩(わきの下)、腹部(お腹の中)、鼠径部(足のつけ根)などのリンパ節の腫れを伴います。リンパ腫によるリンパ節の腫れの多くは、痛みを伴いません。リンパ節やリンパ球は全身に分布しているため、肺、肝臓、脾臓、骨髄、消化管(胃や腸)、乳腺、甲状腺、皮膚、目の周囲、骨など全身のあらゆる臓器へ出現することもあります。時に脳や脊髄などの中枢神経系病変を認めることもあります。リンパ腫による症状の多くは、リンパ腫病変が出現した部位によるため、「リンパ腫に特徴的な症状」はあまりありません。全身症状(B症状といいます)としては、原因不明の発熱、尋常ではないほどの寝汗、急激な体重減少などを伴うこともありますが、それほど高い頻度ではありません。
リンパ腫の診断
リンパ腫の診断は、腫れているリンパ節などを採取して (生検といいます) 顕微鏡で調べる病理組織学的検査が必要不可欠です。病理組織学的検査なしに、症状やCTやPETなどの画像検査、あるいは血液検査だけでリンパ腫を確定診断することは出来ません。リンパ腫はとても多くの病型に分類されます。どのリンパ腫病型か、によって治療方針が異なるため、正確な診断をつけることは、その後の適切な治療方針の決定に最も重要です。リンパ腫は進行・増悪する速度による「悪性度」によって、おおまかに表1のように分類されています(記載している病型は一部です。この他にも多数の病型が存在します)。
| 進行 | B細胞 | T/NK細胞 | |
|---|---|---|---|
| 低悪性度 | 年単位 | 濾胞性リンパ腫、辺縁帯リンパ腫、MALTリンパ腫、リンパ形質細胞性リンパ腫、慢性リンパ性白血病/小リンパ球性リンパ腫 | 菌状息肉症、成人T細胞白血病/リンパ腫(くすぶり型・慢性型) |
| 中悪性度 | 月単位 | びまん性大細胞型B細胞リンパ腫、マントル細胞リンパ腫 | 末梢性T細胞リンパ腫・非特定型、血管免疫芽球性リンパ腫、未分化大細胞リンパ腫、節外性NK/T細胞リンパ腫 |
| 高悪性度 | 週単位 | バーキットリンパ腫、Bリンパ芽球性白血病/リンパ腫 | Tリンパ芽球性白血病/リンパ腫、成人T細胞白血病/リンパ腫(急性型・リンパ腫型) |
リンパ腫の治療
リンパ腫の治療の柱は化学療法(抗がん剤など)ですが、具体的な治療方針は病型によって異なります。インドレントリンパ腫の一部では無治療経過観察(ただちに治療を開始せずに定期的な経過観察を行うこと)や局所治療(放射線治療など)が選択できる場合もあります。アグレッシブリンパ腫以上では、原則として化学療法が勧められます。病型によって、勧められる化学療法の内容(薬剤、治療強度、スケジュールなど)が異なります。また、患者さんの年齢や合併症などの状態によっても投与できる治療内容が異なることがあります。再発時の治療選択肢は多岐にわたります。病型や病状によっては自家造血幹細胞移植併用大量化学療法(自分の造血幹細胞を事前に採取・凍結し、大量化学療法を行った後に解凍して自分へ戻すこと)をお勧めすることがあります。一部の病型では二重特異性抗体の使用が可能です。また、同種造血幹細胞移植(自分以外のドナーさんから、造血幹細胞を移植すること)やCAR-T細胞療法などを検討する場合は、近隣の病院へ連携してご紹介することがあります。患者さんの病状や体調によって治療内容が調整されることがあります。また、それぞれ再発治療には多くの選択肢があります。疾患や病状によって臨床試験や新薬治験の選択肢が存在する場合もあります。具体的には担当医から適切に説明いたします。治療についての疑問点がある場合は、担当医や医療スタッフにいつでも遠慮なくご質問ください。
白血病について
白血病には、急性白血病と慢性白血病があり、さらにそれぞれが骨髄性とリンパ性に大別されます(表1)。主に急性骨髄性白血病 慢性骨髄性白血病 急性リンパ性白血病 慢性リンパ性白血病に大別されます。血液検査、骨髄検査、遺伝子検査、画像検査などによって診断されますが、それぞれの疾患の病態、臨床経過および治療方針は大きく異なります。頻度は少ないですが、他の悪性腫瘍に対する化学療法や放射線治療を受けた患者さんで数年以上を経て白血病を発症することもあります(治療関連白血病と言います)。いずれも治療時には化学療法を行いますが、特に急性骨髄性白血病、急性リンパ性白血病については同種造血幹細胞移植の適応となることがあります。この場合は近隣の病院へ連携してご紹介することがあります。
| 急性 | 慢性 | |
|---|---|---|
| 骨髄性 | 急性骨髄性白血病 | 慢性骨髄性白血病 |
| リンパ性 | 急性リンパ性白血病 | 慢性リンパ性白血病 |
1. 急性骨髄性白血病
病態
骨髄で骨髄芽球とよばれる幼若な細胞が増加し、正常の成熟白血球や赤血球、血小板が減少する疾患です。発熱、倦怠感、紫斑などが初期症状ですが、急激な経過をたどり、生命に関わる状態となるため、迅速な診断、治療導入が望まれます。
治療
強力な寛解導入療法を行い、骨髄検査で寛解を確認したのち、引き続いて地固め療法を行います。染色体・遺伝子検査の結果、適応ある分子標的薬を併用することもあります。若年患者さんの病状によっては同種造血幹細胞移植を検討します。再発・治療抵抗性の患者さんや、高齢の患者さんでは分子標的薬や低用量化学療法を組み合わせた治療が選択されることもあります。疾患や病状によって臨床試験の選択肢が存在する場合もあります。具体的には担当医から適切に説明いたします。治療についての疑問点がある場合は、担当医や医療スタッフにいつでも遠慮なくご質問ください。
急性骨髄性白血病では、一部の治療を除き、原則として入院治療を行います。
2. 急性リンパ性白血病
病態
骨髄でリンパ芽球とよばれる幼若な細胞が増加し、正常の成熟白血球や赤血球、血小板が減少する疾患です。発熱、倦怠感、紫斑などが初期症状ですが、急激な経過をたどり、生命に関わる状態となるため、迅速な診断、治療導入が望まれます。主な治療方針としてはBCR-ABL融合遺伝子陽性のPhiladelphia染色体 (Ph) 陽性急性リンパ性白血病と、Ph陰性急性リンパ性白血病とに大別されます。
治療
Ph陽性急性リンパ性白血病では、分子標的薬であるチロシンキナーゼ阻害剤と化学療法との併用療法を行います。強力な寛解導入療法を行い、骨髄検査で寛解を確認したのち、引き続いて地固め療法、維持療法と施行します。若年患者さんでは同種造血幹細胞移植を積極的に検討します。
Ph陰性急性リンパ性白血病では、強力な寛解導入療法を行い、骨髄検査で寛解を確認したのち、引き続いて地固め療法、維持療法を施行します。若年患者さんでは病状により同種造血幹細胞移植を積極的に検討します。
再発・治療抵抗性の患者さんでは、イノツズマブ・オゾガマイシン、ブリナツモマブなどの抗体薬物複合体や二重特異性製剤を使用することがあります。若年患者さんでは積極的に同種造血幹細胞移植を検討します。疾患や病状によって臨床試験の選択肢が存在する場合もあります。具体的には担当医から適切に説明いたします。治療についての疑問点がある場合は、担当医や医療スタッフにいつでも遠慮なくご質問ください。
急性リンパ性白血病では、維持療法など一部の治療を除き、原則として入院治療を行います。
3. 慢性骨髄性白血病
病態
BCR-ABL1融合遺伝子が原因となり、骨髄で異常な造血の増殖がおこります。慢性期、移行期、急性転化期に分類されますが、慢性期はほとんど無症状で健診などの血液検査で発見されることも多い疾患です。
治療
慢性期の場合(大半の患者さんが該当します)、BCR-ABL1融合遺伝子へ作用するチロシンキナーゼ阻害薬での治療をお勧めします。内服治療のため外来治療が可能で、基本的には入院治療を必要としません。一部の患者さんでは、STAMP阻害薬という、従来のチロシンキナーゼ阻害薬とは異なる作用機序をもつ治療薬をお勧めすることがあります。ほとんどの患者さんではチロシンキナーゼ阻害薬やSTAMP阻害薬への治療反応性は良好であり、これまで通りの日常生活・就労を継続可能です。
骨髄異形成症候群について
骨髄異形成症候群は骨髄中の造血幹細胞に異常が生じて血球の成長に障害が起こり、正常の成熟した血球が造られなくなり、骨髄や血液中に「異型」な血球が出現します。このため、白血球減少、貧血、血小板減少といった「血球減少」が起こります。また、骨髄異形成症候群では未熟な造血細胞(芽球)が増生することがあり、一部の患者さんでは急性骨髄性白血病へ進展することがあります。一般的には高齢者に発症する疾患です。頻度は少ないですが、他の悪性腫瘍に対する化学療法や放射線治療を受けた患者さんで数年以上を経て骨髄異形成症候群を発症することもあります(治療関連骨髄異形成症候群と言います)。画一的な疾患ではなく、骨髄異形成症候群と言っても多様な病態を取ります。具体的には担当医から説明します。
治療
低リスクであれば無治療経過観察、あるいは輸血や造血因子の補充などが検討されます。特徴的な染色体異常(5番染色体の長腕欠損: 5q-症候群と言います)では、免疫調整薬のレナリドミドが使用可能です。
高リスクであれば、DNAメチル化阻害剤や化学療法の導入を行います。若年患者さんの病状によっては同種造血幹細胞移植を検討します。
経過中に急性骨髄性白血病に進展した場合は、急性骨髄性白血病に準じた治療方針が選択されます。
疾患リスクや病状によって臨床試験の選択肢が存在する場合もあります。具体的には担当医から適切に説明いたします。治療についての疑問点がある場合は、担当医や医療スタッフにいつでも遠慮なくご質問ください。
多発性骨髄腫について
多発性骨髄腫は血液細胞の中の「形質細胞」というリンパ球の仲間の細胞ががん化した「形質細胞腫瘍」の最も代表的な疾患です。患者さんは高齢者に多く、女性よりも男性に多い傾向があります。異常な形質細胞が産生する異常な免疫グロブリン(M蛋白と言います)が増加します。発症初期には無症状であることが多く、健康診断の血液検査で高蛋白血症や軽度の貧血・腎障害などで異常を指摘されることも少なくありません。病状が進むと、貧血、血小板減少などの造血障害、腎障害、骨折・骨溶解・骨腫瘤などの骨病変、高カルシウム血症、アミロイドーシス、過粘稠度症候群などを呈することがあります。胸椎・腰椎などの圧迫骨折や病的骨折(通常では骨折しないような軽度の外力による骨折)などで整形外科への受診を契機に多発性骨髄腫の診断につながることもあります。
多発性骨髄腫の診断のためには、血液検査、尿検査、骨髄検査、心電図、心臓超音波、全身単純CT、FDG-PET/CT、レントゲン、MRIなどによる全身精査が必要です。特に骨病変による骨痛や、腎障害などの「臓器障害」を既に認める患者さんでは、診断と治療が急がれます。なお、多発性骨髄腫が疑われた場合、あるいは既に診断されている患者さんでは、造影剤の使用は原則として禁止です(腎傷害が急激に増悪することがあります)。多発性骨髄腫の診断、病態や病状、治療体系は複雑なので、担当医から説明します。
| 多発性骨髄腫の診断規準 |
|---|
以下の2項目を満たす。
|
骨髄腫診断事象
|
| くすぶり型多発性骨髄腫の診断規準 |
以下の2項目を満たす。
|
治療
多発性骨髄腫は一般的に進行が緩慢で長い経過をとる疾患です。近年の著しい治療開発により、その治療成績は確実に改善が続いています。ただし、現時点でもほとんどの患者さんでは「治癒(病気が治ること)」は難しい疾患です。多発性骨髄腫のうち、「くすぶり型」と診断された患者さんでは原則として無治療経過観察が選択されます。活動性のある治療適応の多発性骨髄腫では化学療法の導入が勧められます。
<移植適応の患者さん>
治療適応の多発性骨髄腫では、自家末梢血造血幹細胞移植併用大量化学療法(以下、自家移植と言います)が施行できるかどうかで治療方針が異なります。一般的には若年(65-70歳が上限)で、十分な臓器機能が保たれている患者さんが自家移植の適応となります。まず導入療法を行い、その後自家末梢血造血幹細胞を採取・凍結します。十分な自家末梢血造血幹細胞が採取・凍結されたことを確認し、大量化学療法を投与したのちに、凍結していた自家末梢血造血幹細胞を解凍して輸注します。導入療法の一部(治療開始時)、自家末梢血造血幹細胞採取、および自家移植は原則として入院で行います。
<移植非適応の患者さん>
自家移植の適応とならない高齢患者さんや、何らかの臓器障害を有する患者さんでは化学療法を行います。抗CD38抗体併用化学療法の開発および臨床導入により、移植非適応患者さんの治療成績は確実に向上しています。
再発時にはさらに複数の治療選択肢があります。病態や病状によって臨床試験の選択肢が存在する場合もあります。具体的には担当医から適切に説明いたします。治療についての疑問点がある場合は、担当医や医療スタッフにいつでも遠慮なくご質問ください。
Chapter.3: 頭頸部がんに対する薬物療法
当科では頭頸部領域のがんに対して化学療法を行っています。
従来から、外科医(耳鼻科、頭頸部外科、口腔外科)が化学療法も行う事が多いがんですが、当院では腫瘍内科医(化学療法専門医)が化学療法・分子標的療法・免疫療法を行っています。
この領域のがんの特徴としては総合腫瘍科(腫瘍内科)、頭頸科(外科)、放射線治療科の3科が合同で治療を行う事が多いのが特徴です。
例えば、最も多い頭頸部扁平上皮癌の場合、進行した腫瘍に対しては先ず総合腫瘍科が化学療法を行って腫瘍の縮小をはかり、その後放射線治療部と総合腫瘍科が共同で放射線治療と化学療法を同時に行い、その後に腫瘍が残存する場合には頭頸科で外科的処置をする事があります。
最も多いのは放射線治療部と総合腫瘍科が共同で放射線治療と化学療法を同時に行って治癒を目指す化学放射線療法です。また、頭頸部外科医が手術を行ったあと再発を予防するために化学放射線療法を行う場合もあります。
どの治療方法を選択するかは総合腫瘍科、頭頸科、放射線治療部、更に放射線診断医や看護師らが参加するCancer boardにおいて議論され、患者さんに十分説明して決定されます。
頭頸部扁平上皮癌の治療方針の大略を図に示します。
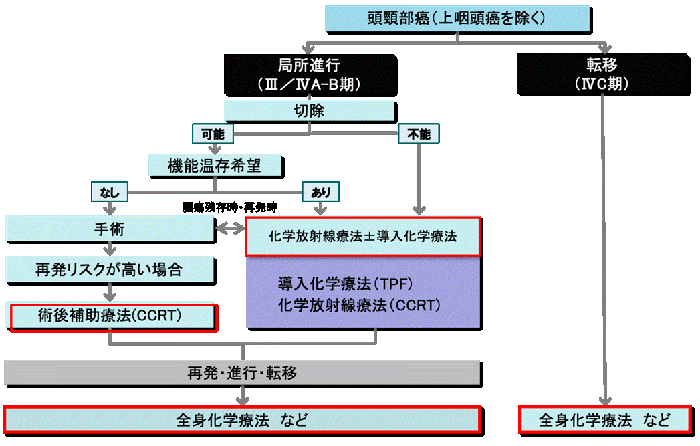
主な頭頸部扁平上皮癌に対する主な薬物療法を以下に示します。これらは大規模な比較試験により評価が確立している標準治療であり、患者さんの全身状態、病変、これまでの治療経過などにより実際の治療は異なる場合があります。(薬剤の用量は標準です。年齢、体力などにより減量する場合があります。
- 導入化学療法:DCF(またはTPF) 3-4週毎に3サイクル
Docetaxel (ドセタキセル) 75mg/m2 d1 CDDP (シスプラチン) 75mg/m2 d1 5-FU (フルオロウラシル) 750mg/m2 D1-5 - 化学放射線療法(CCRT):CDDP 3週毎に3サイクル投与、放射線は毎週5回(月曜−金曜)照射で33-35回
3週ごと投与
毎週投与CDDP (シスプラチン) 100mg/m2 d1
CDDP (シスプラチン) 40mg/m2 d1 - 転移再発症例に対する化学療法
Pembrolizumab + FP 3週ごと (FP 6サイクルまで)
Pembrolizumab 3週ごとPembrolizumab (ペムブロリズマブ) 200mg d1 CDDP (シスプラチン) 100mg/m2 d1 5-FU (フルオロウラシル) 1000mg/m2 D1-4
FP+Cetuximab 3週ごと (FP 6サイクルまで)Pembrolizumab (ペムブロリズマブ) 200mg d1 Cetuximab (セツキシマブ) 初回 400mg/m2, 以降250mg/m2 d1, 8, 15 CDDP (シスプラチン) 100mg/m2 d1 5-FU (フルオロウラシル) 1000mg/m2 D1-4
以上の治療で効果がない場合にはCancer boardで検討し、手術療法、放射線療法などの局所治療に移行するか、あるいは別の化学療法(2nd line以降)を行うか、あるいは新薬の治験等を試みるかについて相談して決定します。
比較的稀な疾患としては唾液腺がん、悪性黒色腫、成人の横紋筋肉腫、神経芽細胞腫などがあげられます。特に後ろのふたつの疾患は成人では稀な疾患であり、がん研有明病院ではこのような稀な疾患の患者さんが全国から集まってきています。
Chapter.4: 原発不明がんに対する薬物療法
当科では原発不明がんの診断、治療も行っています。
原発不明がんとは、病理学的に(腫瘍のサンプルを取って顕微鏡で)悪性と確認された転移性(全身的に広がっている)腫瘍で、通常の血液や画像検査で原発が分からないものを言います。頻度は意外に高く、一般的には悪性腫瘍全体のうち数%を占めると言われます。
診断はまず病理組織検査を詰めることで、以下のような免疫組織染色によって特定の原発巣を推定できる場合があります。
| 組織型 | 抗原(抗体) |
| 癌(上皮性悪性腫瘍) | CK (cytokeratin), EMA, CEA |
| 肺癌 | Napsin-A, TTF-1 |
| 乳癌 | GCDFP-15 |
| 胚細胞腫瘍 | PLAP, c-kit, Oct4, CD30, AFP, hCG |
| 神経内分泌腫瘍 | Chromogranin, synaptophysin, CD56 |
| 肉腫(サルコーマ) | Vimentin, CD34, desmin, myoglobin SMA (smooth muscle actin), S-100 |
| 悪性黒色腫 | S-100, HMB-45, melan-A |
| 中皮腫 | Calretinin, D2-40, mesothelin, WT-1 |
| 中枢神経系腫瘍 | GFAP, neurofilament protein |
最近は腫瘍組織の遺伝子プロファイルを見て原発推定、治療方針決定を行う試みも行われていますが、まだ研究段階です。当院でも原発不明がんの全ゲノム遺伝子解析の研究を行っています。
原発不明がんの中の一部は予後良好群(特定の治療方針によって長期の生存が期待できる群)と呼ばれる患者さんがいます。この場合、原発は確定しなくとも推定されるがん種に応じた治療を行えば治癒、あるいは数年以上の生存が得られる可能性があります。それ以外の場合は、治癒は困難になり、病状の進み方によっては半年も持たない場合があります。
病理・画像・検査所見により予後良好群を見つけ出し、それ以外の場合は化学療法の適応評価(効果がある程度期待できるかの判定)と今後早めに必要になるかも知れない緩和治療の準備を進めていく事が必要になります。
| ・縦隔・後腹膜正中未分化癌 | -- | 胚細胞腫瘍に準じて |
| ・未分化神経内分泌腫瘍 | -- | 胚小細胞癌に準じて |
| ・腹膜癌 | -- | 卵巣癌に準じて |
| ・女性の腋窩リンパ節転移、腺癌 | -- | 乳癌に準じて |
| ・頚部リンパ節転移、扁平上皮癌 | -- | 頭頚部癌に準じて |
| ・鼠径部リンバ節転移、扁平上皮癌 | -- | 婦人科癌に準じて |
| ・男性の硬化性骨転移、PSA上昇 | -- | 前立腺癌に準じて |
原発不明がんに対する主な薬物療法を以下に示します。原発不明がんはそれ程症例が多くなく、また非常に不均一なので大規模な比較試験により評価が確立している標準治療はなく、施設により種々の治療が行われていますが、一番良く行われているのはプラチナ製剤+タキサンと抗がん剤の組み合わせで、当院では外来で投与可能で患者さんのQOLが比較的保てるTC療法(カルボプラチン+パクリタキセル)を通常行っています。又最近、原発不明癌に対するNivolumab(ニボルマブ)が承認されました。
患者さんの全身状態、病変、これまでの治療経過などにより実際の治療は異なる場合があります。
-
TC療法:原発不明がん(特に腺癌)3週ごと
Carboplatin (カルボプラチン) d1 Paclitaxel (パクリタキセル) d1 -
IP療法:小細胞癌、神経内分泌癌、4週ごと
I: Irinotecan (イリノテカン) d1, 8, 15 P: Cisplatin (CDDP;シスプラチン) d1 -
Nivolumab療法:原発不明がん 3週ごと
Nivolumab (ニボルマブ) d1
以上の治療で効果がない場合には総合腫瘍科カンファレンスで検討し、手術療法、放射線療法などの局所治療に移行するか、あるいは別の化学療法(2nd line以降)を行うか、あるいは新薬の治験等を試みるかについて相談して決定します。
Chapter.5: 肉腫、希少がんに対する薬物療法
当科では肉腫を初めとする希少がんに対して化学療法を行っています。
肉腫は発生部位によりその部位を扱う外科医(整形外科、消化器外科、呼吸器外科、耳鼻科・頭頸部外科、泌尿器科、婦人科など)が化学療法も行う事が多いがんですが、当院ではサルコーマセンターを開設し、肉腫を種々の臓器を専門とする医師や多職種の医療従事者が共同で治療する体制を作っています。その中で腫瘍内科医(化学療法専門医)が化学療法あるいは分子標的療法を行っています。
肉腫の特徴としては希少な上にバラエティに富み、診断が難しいことがあります。従って、肉腫の患者さんは2週間に1度開催される総合腫瘍科医師、担当する外科系医師、放射線科医師、更に病理医、基礎研究者らが参加するサルコーマカンファレンスで議論され、正確な診断に基づいて治療方針が議論され、最終的に患者さんに十分説明して決定されます。
肉腫の大部分を占める軟部肉腫は、まず小円形細胞肉腫とそれ以外の軟部肉腫に分けられます。
- 小円形細胞肉腫:主にユーイング肉腫と横紋筋肉腫で、共に成人では稀な腫瘍です。
どちらも化学療法に対する感受性が高く、小児に準じて強力な化学療法+局所治療(手術、放射線)の組み合わせで治療されます。 - 非小円形細胞肉腫:化学療法あるいは放射線療法に対する感受性は低く、たとえ転移があっても可能ならば手術を行う事を考えます。化学療法剤としては未だにアドリアマイシンおよびイホマイドが標準治療ですが、最近新たな抗がん剤が開発されています。
軟部肉腫に対する主な薬物療法を以下に示します。これらは大規模な比較試験により評価が確立している標準治療であり、患者さんの全身状態、病変、これまでの治療経過などにより実際の治療は異なる場合があります。
-
VDC療法:Ewing肉腫、2-3週ごと
V (ビンクリスチン) d1 D/A (アドリアマイシン) d1 6サイクル目以降 → アクチノマイシンD d1 C (シクロフォスファミド) d1 -
VAC療法:横紋筋肉腫、3-4週ごと
V (ビンクリスチン) d1, 8, 15 A (アクチノマイシンD) d1 C (シクロフォスファミド) d1 -
ADR療法:非小円形細胞肉腫、3週ごと
Doxorubicin (アドリアマイシン) d1 -
イフォスファミド療法:非小円形細胞肉腫、3-4週ごと
Ifosfamide (イホマイド) d1-5 MESNA (ウロミテキサン) d1-5 -
トラベクテジン療法:非小円形細胞肉腫、3週ごと
Trabectedin (トラベクテジン) d1 -
エリブリン療法:非小円形細胞肉腫、3週ごと
Eribulin (エリブリンメシル酸塩) d1, 8 - パゾパニブ療法:非小円形細胞肉腫、毎日経口投与
Pazopanib (パゾパニブ) 連日
以上の治療で効果がない場合にはサルコーマカンファで検討し、手術療法、放射線療法などの局所治療に移行するか、あるいは別の化学療法(2nd line以降)を行うか、あるいは新薬の治験等を試みるかについて相談して決定します。
その他の希少がんとして当科では悪性黒色腫(主に粘膜原発)、肺外小細胞癌・神経内分泌癌、悪性中皮腫(主に腹膜原発)、褐色細胞腫/傍神経節細胞腫、さらに原発不明癌の治療を行っています。
Chapter.6: 前立腺がんに対する薬物療法
当科では前立腺がんに対して化学療法を含む薬物療法を行っています。
前立腺がんは男性に特有の、高齢者に多い病気ですが、50歳代以降から患者が増えてきます。前立腺がんは骨への転移が多く、腰背部痛などで発見されることも珍しくありません。PSA等の腫瘍マーカーが上昇することがよく知られていますが、確定診断は泌尿器科で前立腺生検(針生検)を実施して、病理検査の結果で行います。治療法は、病状に応じて、手術(泌尿器科)や放射線治療(小線源治療、外照射:放射線科)、薬物療法(ホルモン療法、化学療法、分子標的薬など)を行いますが、当科では腫瘍内科医が薬物療法を実施します。
- 転移性去勢(ホルモン)感受性前立腺がん(mCSPC)
トリプレット療法:ドセタキセル+ダロルタミド(ARSI)+ADT(アンドロゲン遮断療法) ※ARSI:アンドロゲン受容体シグナル阻害薬
臓器機能や血液検査の結果等から抗がん剤(ドセタキセル)の使用が特に問題のない方には、上記のトリプレット療法(三剤併用療法)を第一に考えます。一方、抗がん剤の使用が好ましくない方には、アビラテロン、アパルタミド、エンザルタミドといったARSIとADTのダブレット療法(二剤併用療法)を実施します。
- 転移のない去勢抵抗性前立腺がん(M0 CRPC)
ホルモン療法が効かなくなった去勢抵抗性前立腺がんの5年生存率は転移がない場合でも約50%です。M0 CRPCに保険診療で使用できる薬剤は、ドセタキセル、エンザルタミド、アパルタミド、ダロルタミドの4剤で、状況に応じて、前立腺局所に対する治療等も検討します。
- 転移性去勢抵抗性前立腺癌(M1 CRPC)
転移のある去勢抵抗性前立腺がんに対しては、ドセタキセル、アビラテロン、エンザルタミドの3剤に加え、ドセタキセルの使用後であれば、カバジタキセルも使用可能になります。その他、個々に遺伝子検査について検討することになります。詳細については担当医にご確認ください。
- 特定の遺伝子変異がある場合
BRCA2 (あるいはBRCA1 )という遺伝子に変異がみつかった場合、オラパリブ(単剤もしくはアビラテロンと併用)やタラゾパリブ(エンザルタミドと併用)という内服薬の使用が可能です。遺伝子検査のタイミング等については、担当医にご確認ください。
- その他の治療法
がんゲノム遺伝子パネル検査を実施して、TMB-highやMSI-highなどの結果が出た場合は、ペムブロリズマブという免疫チェックポイント阻害薬を使用できます。
また、M1 CRPCで転移が骨のみの場合は塩化ラジウムという放射性物質を含む薬剤の使用も検討されます。詳細は担当医にご確認ください。
Chapter.7: 尿路上皮がんに対する薬物療法
当科では尿路上皮がんに対して化学療法を行っています。
尿路上皮がんは発生部位により、腎盂がん、尿管がん、膀胱がんに大別されます。目で見て分かる血尿や排尿時の違和感などの症状をきっかけにみつかることが多く、早期のがんであれば手術を、血尿や病変部位の痛みのコントロールのためには放射線治療を考慮する場合もあります。当科では腫瘍内科医が、泌尿器科医や放射線科医と連携し、手術の前後や転移・進行した尿路上皮がんに対する薬物療法を行います。
近年、尿路上皮がんでは、従来の抗がん剤に加え、免疫チェックポイント阻害薬(ICI)を用いた免疫療法、がんを認識する抗体に抗がん剤が結合した薬剤(ADC)など新しい薬剤が開発され、効果も非常に期待できるようになっています。一方で、多岐にわたる副作用も現れるようになり、生命に関わる場合もあることから、担当医とのコミュニケーションが非常に重要になります。
主な薬物療法は以下の通りです。
転移を有する、もしくは根治切除不能な尿路上皮がんに対して
- エンホルツマブ・ベドチン(ADC)+ペムブロリズマブ(ICI)併用療法
2024年10月より、当院でも開始している薬物療法です。転移・進行した病気に対して最初に行う薬物療法(一次治療)で、ガイドラインでの推奨度も高く、治療効果も従来のものを大きく上回る結果が臨床試験で報告されています。一方で皮疹やしびれなどの副作用に気をつける必要があります。
- GC+ニボルマブ療法
下記のGC療法(ゲムシタビン(G)とシスプラチン(C)併用療法)とICIを併用する治療法です。腎機能が保たれておりシスプラチンが投与できる患者さんで、転移・進行した病気に対して一次治療の適応になります。
- GC療法/GCb療法
ゲムシタビン(G)とシスプラチン(C)、腎機能がよくない場合は、Cの代わりにカルボプラチン(Cb)という抗がん剤を用いて治療を行います。腎機能障害や骨髄抑制等の副作用に気をつけて実施する必要があります。
- アベルマブ(ICI)維持療法、ペムブロリズマブ(ICI)療法
一次治療のGC療法/GCb療法を4〜6回実施して効果があった場合はアベルマブの2週毎の投与を継続する維持治療を行います。一方、一次治療で十分な効果が得られなかった場合は、ペムブロリズマブを3週または6週間隔で投与します。ともにICIであり、自己免疫疾患に類似した免疫関連有害事象(irAE)に注意しながら治療を継続します。
- エンホルツマブ・べドチン(ADC)療法
アベルマブ維持療法、ペムブロリズマブ療法といった二次治療で十分な治療効果が得られず、病気が進行した場合に三次治療として実施します。4割程度の方で効果が期待されます。投与初期は特に皮疹や味覚障害等、投与期間が長くなってくると手足のしびれ(末梢神経障害)が強くなり、普段の生活に影響が出ることがあるため、注意が必要です。
- エルダフィチニブ療法
FGFR3という遺伝子の変異を持つがんに対して、ICIを含む薬物治療後に病気が増悪した患者さんに対して投与されます。爪の障害や目の障害、血液中のリン濃度の上昇などの副作用を認めることがありますので、皮膚科医、眼科医などとの連携が必要です。
- その他の治療法
特定の遺伝子に変異がある方に対して、治療効果が期待される薬剤が保険診療で使えるようになります。専用の遺伝子検査を行ったり、あるいは、『がんゲノム遺伝子パネル検査』といって、病気の組織の一部や血液等を材料として行う遺伝子検査についても当院で保険診療で実施しています。検査の詳細については担当医にご確認ください。
周術期治療
- dose dense MVAC療法(ddMVAC療法)
筋層浸潤膀胱がんに対して、手術を行う前に実施する抗がん剤治療です。原発病変が大きい場合は、それを小さくして手術を行いやすくするというメリットがあります。また、それだけでなく、全身治療を加えることにより、遠隔転移の再発を抑えたり、生存率を上げる効果が示されています。入院で2週間毎に4回を目標に実施します。
- 術後オプジーボ(ICI)療法
手術後に病理検査の結果等から再発リスクが高いと考えられる方に使用する治療です。2〜4週間間隔でオプジーボを12か月間投与します。
Chapter.8: 腎細胞がんに対する薬物療法
当科では腎細胞がんに対して薬物療法を行っています。
腎細胞がんは、腎臓の細胞ががん化することによって発生するがんで、近年罹患率が増加傾向にあります。進行すると血尿、腹部のしこり、わき腹の痛みと言った古典的な腎細胞がんの「三徴」と言われる症状が現れることもありますが、人間ドックや健康診断などの発達により、約70%の患者さんが無症状で発見されると言われています。
腎細胞がんの治療は、がんの進行度(ステージ)や患者さんの全身状態によって異なります。早期の腎細胞がんでは手術が基本的な治療となります。転移がある場合や手術が困難な場合には、主に薬物療法が選択されます。当科では腫瘍内科医が泌尿器科医と連携し、転移・再発した腎細胞がんに対する薬物療法を中心に行います。
近年、腎細胞がんの薬物療法は大きく進歩しており、分子標的薬や免疫チェックポイント阻害薬(IO)といった新しいタイプの薬剤が登場し、以前と比して治療成績が向上しつつあります。これらの薬剤は、従来の抗がん剤とは異なるメカニズムで効果を発揮し、副作用の種類や現れ方も異なります。そのため、治療中は担当医との綿密なコミュニケーションが非常に重要になります。
主な薬物療法は以下の通りです。
転移を有する、もしくは根治切除不能な腎細胞がんに対して
- 免疫チェックポイント阻害薬(IO)と分子標的薬の併用療法、またはIO同士の併用療法
転移・再発した腎細胞がんの初回治療(一次治療)として、現在最も推奨されている治療法です。免疫の力を利用してがん細胞を攻撃するIOと、がん細胞の増殖や血管新生を抑える分子標的薬を組み合わせることで、より高い治療効果を目指します。また、異なる種類のIOを2剤組み合わせる治療法も選択肢の一つです。
これらの治療法は高い効果が期待できる一方で、免疫関連の副作用(間質性肺炎、甲状腺機能異常、大腸炎、皮膚障害など)や、分子標的薬による副作用(高血圧、手足症候群、下痢、倦怠感など)に注意が必要です。
- 分子標的薬による治療
IOが使用できない場合や、IO治療後の二次治療以降で用いられることが多い治療法です。がん細胞の増殖に関わる特定の分子を標的とする薬剤で、スニチニブ、パゾパニブ、アキシチニブ、カボザンチニブなどが代表的です。これらの薬剤は、がんの進行を遅らせ、症状を和らげる効果が期待されます。
副作用としては、高血圧、手足皮膚反応、下痢、口内炎、倦怠感、甲状腺機能低下などが挙げられます。
- HIF2α(低酸素誘導因子)阻害薬
腎細胞がんの発生メカニズムの一つとして、VHL(フォン・ヒッペル・リンドウ)遺伝子の機能異常が知られています。この異常により、HIF-2α(ヒフツーアルファ)というタンパク質が細胞内に過剰に蓄積し、がん細胞の増殖や血管新生(がんが栄養を得るために新しい血管を作ること)を促進します。
ベルズチファンは、このHIF-2αの働きを直接阻害することで、がんの進行を抑える効果が期待される新しいタイプの経口分子標的薬です。特に、既存の治療法で効果が不十分であった進行性の腎細胞がん患者さんや、VHL病に伴う腎細胞がん患者さんなどに対する新たな治療選択肢として注目されています。
- 免疫チェックポイント阻害薬(IO)による単剤治療
主に二次治療以降で、ニボルマブが単独で用いられることがありますが、近年は多くの場合、一次治療においてIOが使用されるため、二次治療以降でIOが使用される頻度は減っています。がん細胞が免疫細胞の攻撃から逃れる仕組みを解除することで、患者さん自身の免疫力を高めてがんと闘います。
副作用は併用療法と同様に免疫関連の副作用に注意が必要です。
- その他の治療法
上記の治療法が効果不十分な場合や、患者さんの状態によっては、エベロリムスのようなmTOR阻害薬と呼ばれる分子標的薬や、過去に用いられていたインターフェロンαなどのサイトカイン療法が検討されることもあります。
また、特定の遺伝子変異(例:VHL遺伝子変異など)に対する新しい治療薬の研究も進んでいます。『がんゲノム遺伝子パネル検査』によって、個々のがんの遺伝子情報を調べ、最適な治療法選択に役立てることもあります。検査の詳細については担当医にご確認ください。
腎細胞がんの薬物療法は日々進歩しており、患者さん一人ひとりの病状や体力、ライフスタイルに合わせて最適な治療法を選択していくことが重要です。治療内容や予想される副作用、日常生活での注意点などについて、担当医とよく相談し、納得のいく治療を進めていきましょう。



