- HOME
- ����Ɋւ�����
- ����̎�ނɂ���
- �̑�����
�̑�����
���L���a�@�̊̑�����f�Â̓���
���L���a�@�̊̑�����f�Â̓���
�f��
1�D�`�[�����
�̒_�X���ȁA�̒_�X�O�ȁA�摜�f�f����a�����Ȃǂ��܂߂�“�`�[���̒_�X”�Ƃ��āA���҂���ɓK�������Â��l���A���܂��B���ɓ��ȂƊO�Ȃ͓����a���ɋΖ����Ă���A��ɏ��������Ȃ���f�Â��s���Ă��܂��B
2�D�f�f�A����
�̍זE���̎��ẤA�J���E���o����p�A�o��I���h�ɂ��Ďp�A�J�e�[�e����p�����ǐ��p�A�Ö@�ȂǑ���ɂ킽��܂��B���@�ł́A���f�̌�A���₩�ɐi�s�x��̋@�\���܂߂��S�g��Ԃ̕]�����s���A���Ö@���������܂��B���Ì�������ɂ킽���čĔ����J��Ԃ����Ƃ��̍זE���̓����ł���A����I�Ȍo�ߊώ@���s���A�Ĕ��ɑ��Ă��A���̓s�x�K�������Ö@�����悤�ɓw�߂Ă��܂��B
�]�ڐ��̎�ᇂ̎��Âɂ͎�p�ƖÖ@������A���Ƃ̂������舵���f�ÉȂƊ̒_�X�O�ȂƂ̍��c�ɂ�莡�Õ��j�����肵�Ă��܂��B
3�D�����ƗՏ��̉˂���
����f�Â̌���̂��߂ɁA���҂���̎���I�Ȃ����͂ɂ��Տ������͕s���ł��B�f�f�E���Âɂ�����ƂƂ��ɁA���ӂ̂������������҂���Ɋւ��ẮA�V�������Ö@���p��Z�Ȃǂ̗Տ��������ϋɓI�ɍs���Ă��܂��B
����
1�D�a�Ԃɉ�������؏��Ö@
���Ȃł͎�Ƃ��āA�o��I���W�I�g�ĎܗÖ@�iRFA�j��̓����ǐ�Ö@(TACE)�ɉ����āA�Ö@��S�����Ă��܂��BRFA�̑ΏۂƂȂ邪��̑����́A����̏�ԂƂ��Ă͎�p�\�ȕa�ςł���A��������̋@�\�Ȃǂ��l�����Ċ̒_�X�O�ȂƂ̍��c�Ŏ��Ö@�����肵�Ă��܂��B�܂��A�Ǐ����䂪����ȑ�������ɑ��ẮA������h�{�Ƃ��錌�����ɎՒf����TACE���傽�鎡�ÂɂȂ�܂��B����ATACE�s���̂����̊O�]�ڂ�����̏ꍇ�́A�Ö@�̑ΏۂɂȂ�܂��B�����̎��Ö@�́A����̋Ǎ݂݂̂Ȃ炸�A����ݏo���̑��̏�Ԃɂ���Ă��قȂ�A���Ɋ̍d�ς��������Ă���ꍇ�́A�T�d�ȑΉ����K�v�ł��B���@�ł́A���ȁE�O�ȁE�摜�f�f���Ƃ̍��c�̉��A���҂���ɓK�������Â��Ă��Ă��܂��B
2�D���L���ȖÖ@�̒Nj�
���̐��N�A�̍זE���ɑ��ĐV���ȖÖ@�����X�ɓK�����擾���Ă��܂����B�������Ȃ���A������̎��Ö@���ꎟ���ÂƂ��Ă�10�N�ȏ�O�̕W�����ÂƂ̔�r�����A���Èȍ~�͖����ÂƂ̔�r�����̌��ʂ��Ă̓K���擾�ł���A�ǂ̖Ö@���ł��K���Ă��邩�͍��Ƃ�Ƃ����ƂȂ��Ă��܂��B�܂��A�L�]�ȖÖ@���o�ꂵ�����ƂŁA�]����TACE�Ƃ̐��ݕ�������������Ă���A���܂��܂ȑg�ݍ��킹���l������悤�ɂȂ��Ă��܂��B�������������邽�߂ɂ́A�����̕a�@�����͂��đ吨�̊��҂���̎Q���̂��Ƃɍs����Տ��������s���ł��B���@�ł́A��ɍŗǂ̕W�����Â��ɂ���ƂƂ��ɁA���{�����Տ������⎡���i��Ǝ哱�Տ������j�ɂ��ϋɓI�ɎQ�����A����l�̎��Â�ʂ��āA��葁���A�����̊��҂���ɐV���Ȏ��Ö@���Ҍ����邱�Ƃ�ڕW�Ƃ��Ă��܂��B
�O��
1�D������߂Ȃ��O��
�������Őf�f�\�ȏ����ǂ̂���ƈقȂ�A�̂���E�_������E�X����̐i�W���摜�����Ŕ��f���邱�Ƃ͎��ɍ���Ȃ��Ƃ�����܂��B�܂���p�K���i�؏��\���ǂ����̔��f�j���{�݂ɂ��قȂ�̂�����ł���A����a�@�Ŏ�p���ł��Ȃ��Ƃ����Ă��ʂ̕a�@�ł͎�p���ł���Ƃ������Ƃ��H�ł͂���܂���B��p�̌o����Z�ʂ̂ق��A��t�̍l�������傫����p�K���ɉe������̂��̒_�X�O�Ȃ̗̈�ł��B��X�́A�����ł����Ă��O�ȓI�ȗ��ꂩ��̉\�����Ō�܂ŒNj����܂��B“������߂Ȃ��O��”�����b�g�[�Ƃ��A���҂���ƂƂ��ɁA����ɗ����������ĎQ��܂��B
2�D�o���̏��Ȃ���p��S�����Ă��܂�
�̂���E�_������E�X����́A���Ȃ��̒��̍ł����G�ȕ��ʂɂł��邽�߁A��p�����ɕ��G�Ő؏�������ł���A�o���ʂ������Ȃ肪���ł��B�������O�Ȉ�̏K�n������Z�ɂ��܂��܂Ȉ�Ë@���g�ݍ��킹�邱�ƂŁA��p���̏o�����ł��邾�����Ȃ��Ȃ�悤�H�v���Ă��܂��B�o���̂����Ȃ���p�͈��S�����m�Ȏ�p�ɂȂ���܂��B���ǂ���������ɐ؏�����g���p���畠�o����p�Ƃ������ɏ��������łł����p�܂ŁA�X�̊��҂���̕a��ɍ��킹���ߕs���̂Ȃ���p���@��I�����Ă��܂��B
�̑�����̎��Â̎���
�O�Ȏ��Â̎���
�̍זE���̐؏��ɂ́A�n���I�̐؏��ƌĂ���ᇂɂ�����߂��喬�̗����̈�̊̑���؏�����p���ƁA�̑g�D���ł��邾����������̕����؏���2��ނ�����܂����A��ᇂ̏�Ԃ�̋@�\�Ȃǂ��l�����āA���ꂼ��̊��҂���ɓK�����؏��̎d����I�����Ă��܂��B���o�����̐؏����K���ƂȂ鎖������܂��B2022�N�܂ł̊̍זE���؏���p�����ƁA����܂łɍs�����̍זE���̎�p��̐������������܂��B
�݂����咰����ȂǁA���̑���ɂł�����ᇁi�������j�����ᇍזE����Ɍ��t�̗���ɏ���Ċ̑��ɂ��ǂ蒅���A�����ő��B�����]�ڐ��̎�ᇂ́A������ᇂ̐����ɂ���Ă͊O�ȓI�؏����悢���Ö@�ɂȂ�ꍇ������܂��B���@�ł́A�O�ȓI�؏��Ő����\��̉��P�������߂�咰����Ɛ_�o�������ᇂ̊̓]�ڂɑ��ẮA�ϋɓI�Ɏ�p���s���Ă��܂��B����A��ᇂ̐��⌴������̎�ᇂ̏ɂ���ẮA�݂���E������E�t����E��������A������GIST�Ƃ�������ǂ̓���Ȏ�ᇂ���̊̓]�ڂ��A�O�ȓI�؏������҂���̃����b�g�ɂȂ邱�Ƃ�����A�\���Ɏ�ᇂ̏�]��������Ŏ�p���s���Ă��܂��B�܂��A�X����E�_������E�x����ȂǁA���ɐi�s�������A����܂Ŋ̓]�ڂ̐؏��ΏۊO�Ƃ��Ă�������ɑ��Ă��A�ߔN�̉��w�Ö@�̐i���ɂ��A���w�Ö@���ǂ��������ꍇ�ɊO�ȓI�؏����s���A�ǍD�Ȍ��ʂ������銳�҂����X�ɑ����Ă��Ă��܂��B
���Ȏ��Â̎���
2015�N����2024�N�܂łɊ̍זE���ɑ��Ď{�s�������Ȏ��Â̐��ڂ������܂��B2018�N���g�p�\�Ȗ�܂������A2021�N����͖Ɖu�`�F�b�N�|�C���g�j�Q���p�����Ö@���s����悤�ɂȂ��Ă��܂����B�����̖Ö@�̐i���ɂ��A�̓������w�ǐ�Ö@�iTACE)�̌��ʂ��\���Ɋ��҂ł��Ȃ��ꍇ�ɂ́A��葁���i�K����Ö@�ɐ�ւ���悤�ɂȂ��Ă��܂��B
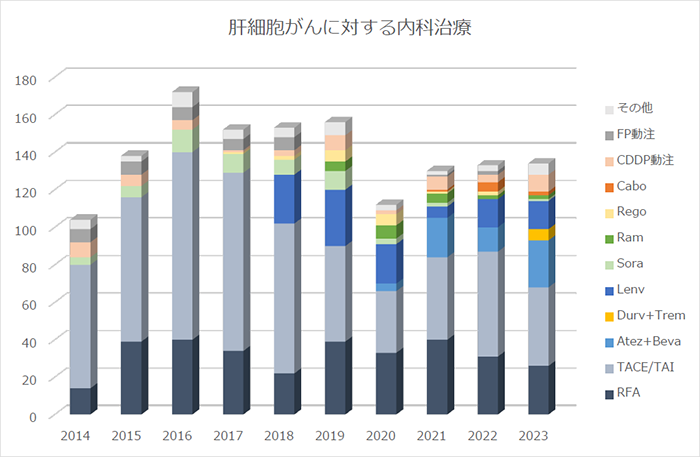
���L���a�@�̊̑�����
�̍זE����ɂ��Ă̒m��
�̑�����Ƃ�
�̑��͐��l��800�1200g ����l�̍ő�̑���ł��B�̑��́A���t���h�߂��ėL�Q��������菜���Ă����ւƂ��đ̊O�ɔr��������A�H�����̎��b�̏�����������_�`�債����A�G�l���M�[�̏���ɕK�v�ƂȂ�O���R�[�Q���i�����j�������肷�铭����S���Ă��܂��B
�̑��ɔ������鈫����ᇂɂ́A�̑����̂��̂ł����܂��u�������v�̂���ƁA���̑��킩�炪��זE���ڂ��Ă��Ċ̑��Ŕ��炵�Ăł���u�]�ڐ��v�̂���Ƃ�����܂��B�������̂���͂���ɁA�̑����\������זE�̈Ⴂ�ɂ��A�u�̍זE���v�Ɓu�̓��_�NJ��v�ɕ������܂��B�������邨�����Ƃ̍זE�̈Ⴂ�ɂ��A�o���オ������ᇂ̐��i�������قȂ��Ă��܂�����A���Â���ꍇ�ɂ͂����������Ⴂ�ɔz������K�v������܂��B�̓��_�NJ��ɂ��ẮA�_������̍����Q�Ƃ��������B
�������̂���![�]�ڐ��̊�](images/liver_iimg02.gif)
�]�ڐ��̂���
�̍זE��
���{�ɂ����āA�̍זE���̖�75%��B�^���邢��C�^�����̎����ɗR�����܂��B���̑��A�A���R�[���ێ��i�������̌����ƂȂ�܂����A�ߔN�A����ɔ�A���R�[�������b���̉�(NASH)����������q�Ƃ��Ē��ڂ���Ă��܂��B�N��ʂɂ݂��̍זE���̜늳���i�a�C�ɂ����銄���j�́A�j���ł�45����A�����ł�55���瑝�����܂��B�늳���E���S���Ƃ��j���������̖�3�{�����ł��B�늳���Ǝ��S���̔N�����ڂ܂ꂽ�N��ʂɌ���ƁA�j���Ƃ�1935�N�O��ɐ��܂ꂽ�l�ō����Ȃ��Ă��܂��B����́A1935�N�O��ɐ��܂ꂽ�l�̑������̍זE���̗v���ł���C�^�̉��Ɋ������Ă��邱�ƂƊ֘A���Ă��܂��B�늳���̍��۔�r�ł́A���{���܂ޓ��A�W�A�n�悪�����Ȃ��Ă��܂��B����́A���{���������A�W�A�n��̐l�̑������̍זE���̗v���ł��� B�^�̉��Ɋ������Ă��邱�ƂƊ֘A���Ă��܂��B�ߔN�ł́AC�^�̉��̗\�h�Ǝ��Â̐i���ɂ��AC�^�̉��R���̊̍זE���̜늳���E���S���Ƃ��������A����ƂƂ��Ɋ̍זE���S�̜̂늳���E���S���������X���ɂ���܂��B
�]�ڐ��̂���
�]�ڐ��̂���́A�ǂ����ʂ̕��ʂ̌�����ᇁi���Ƃ��Έ݂����咰����Ȃǁj����̑��ւ̓]�ڂł��̂ŁA���̌�������̕a���ł̓X�e�[�W�W�ɑ������܂��B�̓]�ڂ́A��ᇍזE����Ɍ��t�̗���ɏ���Ċ̑��ɂ��ǂ蒅���A�����ő��B���邱�Ƃɂ���ċN����܂��B���Â͑S�g�����w�Ö@�i�R����܂̑S�g���^�j����ʓI�ł����A��������̐����ɂ���Ă͎�p�Ȃǂ̋Ǐ��Ö@���悢���Ö@�ɂȂ�ꍇ������܂��B
�Ǐ�
�̑��͒��ق̑���Ƃ������A���ł��Ă���قǐi�s���Ȃ�����͏Ǐ�����܂���B�i�s����Ƃ݂������Ɍł������܂��G�ꂽ��A���ɔj��ƓˑR�̋����ɂ݂�n���̐i�s���݂�ꂽ�肷�邱�Ƃ�����܂��B�ʏ�͎��o�ł���Ǐ�͂قƂ�ǂȂ��A����Ƃ������͊̉��E�̍d�ςȂNJ̑���Q�ɗR������Ǐ�ƍl�����܂��B�����̑����͐H�~�s�U�A�S�g���ӊ��A�����c�����Ȃǔ��R�Ƃ����Ǐ�ŁA�̍זE�����^�����R�Ƃ��Ă͎ア���̂ł��B���t��f�����Ȃǂ͐i�s�����̍d�ς̏Ǐ�ł���A�̍זE���̔����ɖ��ɂ��Ƃ͂����܂���B
�f�f
B�^�����̉��EC�^�����̉��E�̍d�ς̂����ꂩ�����݂���A�̍זE���̍��댯�Q�ł���A��������̑ΏۂƂȂ�܂��B���ł�B�^�̍d�ς�C�^�̍d�ςƌ����Ă�����́A�����댯�Q�Ƃ��Ă��ׂ��Ȓ���������K�v�ł��B�ߔN�AC�^�̉��E�C���X�̋쏜���Â��ϋɓI�ɍs����悤�ɂȂ�A�E�C���X�A�����ƂȂ����ꍇ�ɔ����̒ቺ���F�߂��Ă��܂����A����ŁA�E�C���X�쏜�ɐ����������ƂŒ�������𒆒f�������ʁA�̍זE�����傫���Ȃ��Ă��甭�������P�[�X���U������A���ƂȂ��Ă��܂��BC�^�̉��E�C���X���A�����ƂȂ����ꍇ�ł��A����I�Ɍ��t�����Ɖ摜�������p�����邱�Ƃ����������߂��܂��B����AB�^�̉���C�^�̉��ȊO�̕��̏ꍇ�A���f�ł̊̋@�\�ُ��A���̑��̈�ʓI�ȑ̒��s�ǂŕa�@����f�����ۂ̌����ُ���_�@�Ɋ̍זE�����݂���Ƃ����p�^�[���������Ǝv���܂��B
���t�����ł́AAST(GOT)��ALT(GPT)�Ƃ������̑��R���̍y�f�����A��������A���u�~���A�v���g�����r��(PT)���ԂƂ������̋@�\������킷���ڂɒ��ӂ��A�̏�Q�̒��x�����邱�Ƃ��d�v�ł��B�̍d�ς��^����A�̍זE���̍��댯�Q�Ƃ��āA���ׂ��Ȓ�������̑ΏۂƂȂ�܂��B�̍זE���ŏ㏸�����ᇃ}�[�J�[�Ƃ��āAAFP��PIVKA-II�Ȃǂ�����܂��B�����̃}�[�J�[�l���������Ƃ́A�̍זE�����^���v�f�ɂȂ�܂����A����ȊO�ł������Ȃ邱�Ƃ�����A���ӂ��K�v�ł��B
�摜�f�f�ł����Ƃ���y�Ȃ͕̂��������g�����ł��B���҂���ɕ��S�Ȃ��s����̂����_�ł����A�̑��̒��̎�ᇂ̏ꏊ�ɂ���Ă͌����Ȃ����Ƃ�����܂��B�摜�f�f�ōł��M�����������̂��A���e�܂�p����CT��MRI �ł��B
�T�[�x�C�����X�E�f�f�A���S���Y��
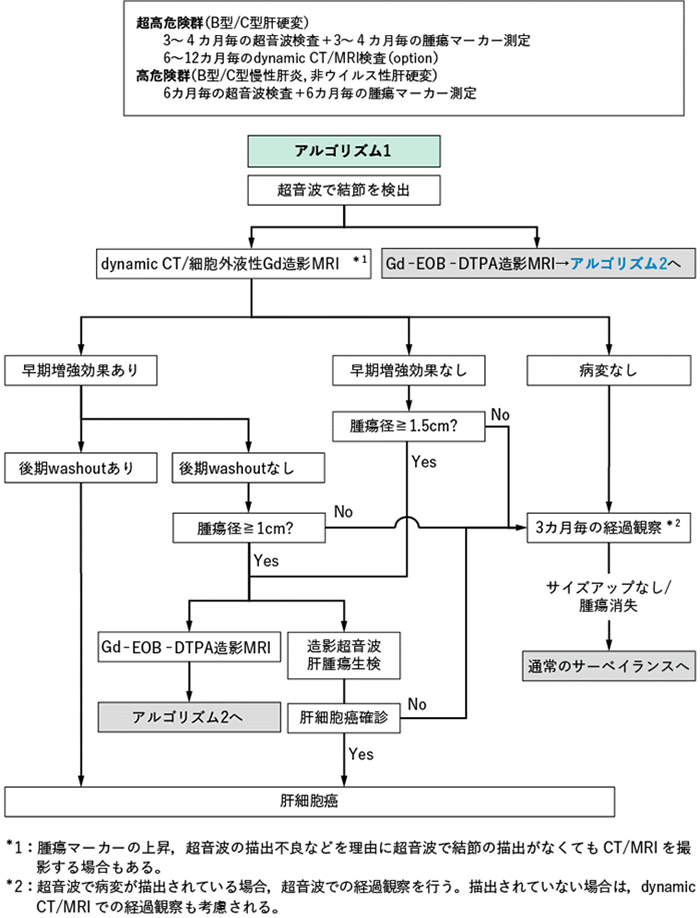
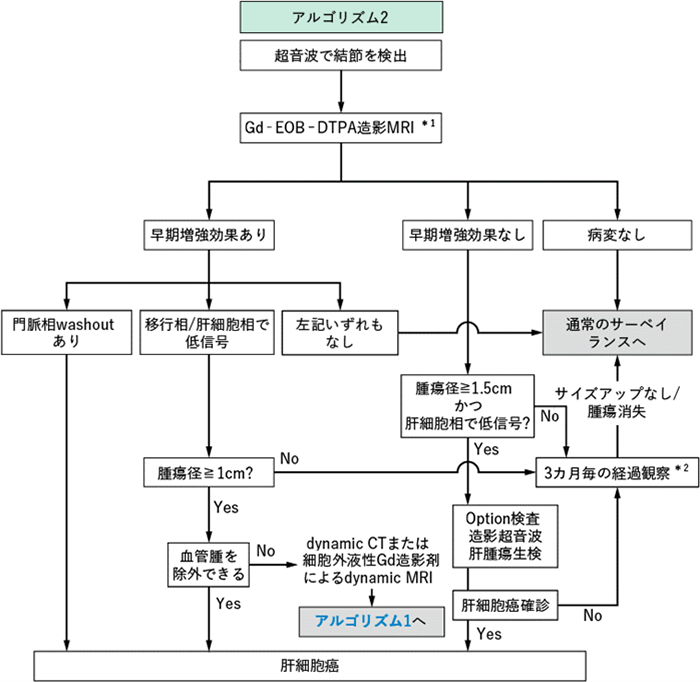
�i�̊��f�ÃK�C�h���C��2021���, ���{�̑��w��쐬, ���{�����Êw��HP���]�ځj
�a���f�f
�̍זE���̕a�����ނɂ́A���ە���(���ۑ���A��:UICC�A��8��)�ƍ������ށi�̊��戵���K��A��6�Łj������܂��B��������A��{�� �̓��a�ς̏iT���q�j�A�̑��ߖT�̃����p�ߓ]�ڂ̗L���iN���q�AN1�F�]�ڂ���j�A���u�]�ڂ̗L���iM���q�AM1�F�]�ڂ���j����\������܂����A���҂���v���Ȃ�����������܂��B�X�e�[�W�̘b������Ƃ��́A�ǂ̕��ޖ@��p���Ă��邩�ɒ��ӂ��K�v�ł��B
�̍זE���̎��ẤA���҂��g�̊̋@�\�ɂ���đ傫�����E����܂��B���������āA����̕a���f�f�ƂƂ��Ɋ̏�Q�x���q�ϓI�ɕ]������K�v������A�̊��f�ÃK�C�h���C���ł́AChild-Pugh���ނ��p�����Ă��܂��B
�܂��A����f�Âł́A����̐i�s�x�Ɗ̏�Q�x��g�ݍ��킹���A������u�����X�e�[�W���O�v���p�����Ă��܂��B�����X�e�[�W���O�͂��낢��Ȏ{�݂���l�X�Ȃ��̂��o�Ă���A�ǂ̕��ޖ@���D��Ă��邩�̕]���͒�܂��Ă��܂���B��r�I�悭�p�����Ă��镪�ނƂ��āA�o���Z���i�Տ��̊��iBCLC�j�a�����ނ������܂��B
| T | N | M | |
| Stage I A | T1a | N0 | M0 |
| Stage I B | T1b | N0 | M0 |
| Stage II | T2 | N0 | M0 |
| Stage III A | T3 | N0 | M0 |
| Stage III B | T4 | N0 | M0 |
| Stage IV A | T1�`4 | N1 | M0 |
| Stage IV B | T1�`4 | N0�`1 | M1 |
| T1a: 2cm�ȉ��C�P�� T1b: 2cm���C�P���C���ǐN�P�Ȃ� T2: 2cm���C�����C���ǐN�P����C�܂��� 5cm�ȉ��C���� T3: 5cm���C���� T4: �喬�������͊̐Ö��̑啪�}�ւ̐Z��, �_�X�ȊO�̗אڑ���ւ̒��ڐZ���C �܂��� �����������ђ� |
|||
| T | N | M | |
| Stage I | T1 | N0 | M0 |
| Stage II | T2 | N0 | M0 |
| Stage III | T3 | N0 | M0 |
| Stage IV A | T4 | N0 | M0 |
| T1�`4 | N1 | M0 | |
| Stage IV B | T1�`4 | N0�`1 | M1 |
| T: �@��ᇌ��F�P���C�A��ᇌa�F2cm�ȉ��C�B���ǐN�P�Ȃ��C�̂����A T1: 3���ڑS�č��v�CT2: 2���ڍ��v�CT3: 1���ڍ��v�CT4: �S�č��v���� |
|||
| 1�_ | 2�_ | 3�_ | |
| �]�� | �Ȃ� | �y�x | �Ƃ��ɍ��� |
| ���� | �Ȃ� | ���� | ������ |
| �����r�����r���l(mg/dl) | 2.0���� | 2.0�`3.0 | 3.0�� |
| �����A���u�~���l(g/dl) | 3.5�� | 2.8�`3.5 | 2.8���� |
| �v���g�����r�������l(%) | 70�� | 40�`70 | 40���� |
| Child-Pugh����: �e���ڂ̃|�C���g�̍��v�_�ŕ��ނ��� A 5�`6�_, B 7�`9�_, C 10�`15�_ |
|||
| �X�e�[�W | �S�g��� | �̏�Q�x | ���̏�� |
| ������(0) | �ǍD | A | �P��, 2cm�ȉ� |
| ����(A) | �ǍD | A-B | �P���`3cm 3�ȓ� |
| ���Ԍ^(B) | �ǍD | A-B | ���� |
| �i�s��(C) | ���s�� | A-B | �喬�Z��, �̊O�]�� |
| �I����(D) | �s�� | C |
���Ö@
�̊��f�ÃK�C�h���C���ł́A�̏�Q�x�Ǝ�ᇂ̃T�C�Y����ɉ����āA�̐؏��E���W�I�g�Ȃǂ̋Ǐ����ÁA�̓����ǐ��p�A�S�g���w�Ö@�A�̈ڐA�A�ɘa�P�A��I�����邱�Ƃ�����Ă��܂��B�X�̊��҂���ɂ����ẮA��ᇂ̏ꏊ�∫���x�i���ǂZ�����Ă��邩�Ȃǁj�Ƃ��������������܂��A���Õ��j�����肵�܂��B
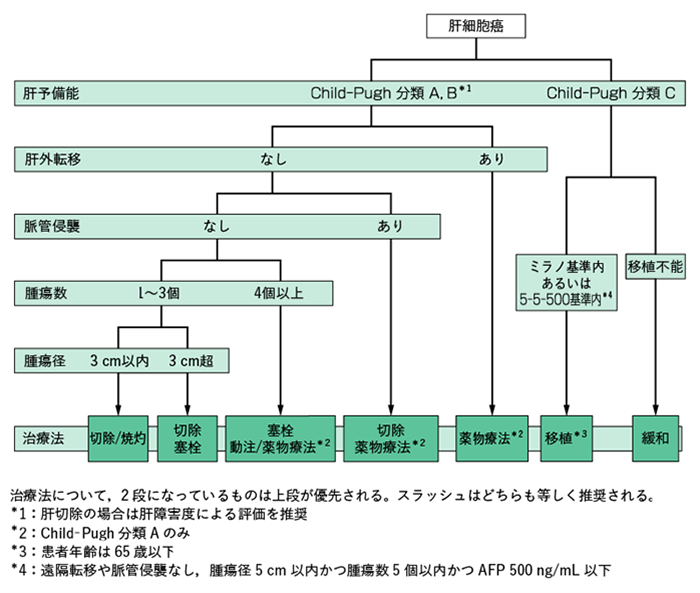
�i�̊��f�ÃK�C�h���C��2021���, ���{�̑��w��쐬, ���{�����Êw��HP���]�ځj
��p�Ö@
�ł��m���Ȏ��Ö@�́A�O�ȓI�؏����ƍl���Ă��܂��B�̋@�\���ǂ���A��r�I�傫�Ȃ���ł��؏����\�ł��B�̍זE���̐؏��ɂ́A�n���I�̐؏��ƌĂ���ᇂɂ�����߂��喬�̗����̈�̊̑����ꊇ���Đ؏�����p���ƁA�̑g�D���ł��邾����������̕����؏���2��ނ�����܂��B��ᇂ̏�Ԃ�̋@�\�Ȃǂ��l�����āA���ꂼ��̊��҂���ɍœK�Ȑ؏��̎d����I�����Ă��܂��B��ᇂ̈ʒu��傫���ɂ��܂����A���o�����̐؏����ϋɓI�ɍs���Ă��܂��B
�o��I���W�I�g�ĎܗÖ@(RFA�j
�����g�i�G�R�[�j�Ō��Ȃ����ᇂɓd�ɐj���h���A���W�I�g�d���𗬂����Ƃɂ��A�d�Ɏ��͂ɔ����������M�ɂ���ᇂ������鎡�Ö@�ł��B5�`10���̉��M�ɂ�蒼�a2�`3cm�̋���͈̔͂��Ìł���܂��̂ŁA���͈̔͂Ɋ��S�Ɏ��܂鏬���Ȃ��ł��ǂ��K���ɂȂ�܂��B3cm���x�ɂȂ�ƁA�Ӊ��Ɏ��Â��s�\���ȏꏊ���c��Ȃ��悤�ɁA�j�����������炵�ĕ�������M���܂����A���Â̊m�������ቺ���܂��B�ߔN�̗Տ������ŁA�m���ɏĎ܂ł���悤�ȏ��a�ςł���Ύ�p�Ɠ����̎��Ì��ʂ������邱�Ƃ��m�F����܂����̂ŁA���ɍ���̕��Ȃǂł�RFA�𐄏����邱�Ƃ������Ă��܂��B���̂ق��A�؏���̍Ĕ���A�̏�Q�xB�Ȃǎ�p������RFA�̑ΏۂƂȂ�܂��B�o�߂������ȏꍇ�͎��Â�4-5����ɑމ@�\�ł����A�o���i���o���E���o���E�_���j��̍[�ǁA�̔^ᇁA�M�ɂ����ӑ����Q�ȂǏd�Ăȍ����ǂ��N���肦�܂��B
- RFA�̎��Ð���
�����ł̑��{�ݗՏ������̌��ʂƂ��āA�̋@�\�ǍD��3cm 3�ȓ��̏����̍זE���Ǘ�ɑ���ARFA��3�N���Ĕ���������47.7%�ƕ���Ă��܂��B
�̓������w�ǐ�Ö@�iTACE�j
����̊̑��́A�̓�������і喬���炻�ꂼ��2����8���̌������܂����A�̍זE���͊̓����݂̂���e�����܂��B���̐����𗘗p���A������h�{����̓�����ʂ��čR����܂ƍǐ��𒍓����邱�ƂŁA����̂ւ̃_���[�W���Œ���ɂ��Ȃ��炪����U���E���ƍU�߂ɂ��鎡�Â�TACE�ł��B1�{�̌��ǂ��ǐ����邱�Ƃɂ��A���̌��ǂ���h�{����������邪����Ɏ��Âł��邱�Ƃ���A��p��RFA���s�����̑����a�ς��ǂ��K���ł��B�����̌��ǂ���h�{����ꍇ��A��^�̂���̏ꍇ�ɂ́A��x�ɍǐ����s���ƁA����̂ւ̃_���[�W���ᇕ���ɂ��_���[�W���傫���Ȃ邱�Ƃ�����A�v��I�ɕ�����ɕ����Ď��Â��s�����Ƃ�����܂��B�܂��A�̋@�\�������ꍇ�ɂ́A�����ǐ��݂̂ł��̕s�S�ɐi�s���邱�Ƃ�����A�R����܂݂̂𒍓����铮�����w�Ö@(TAI)���s�����Ƃ�����܂��B
- TACE�̎��Ð���
�����̗Տ������̃��r���[�Ƃ��āA�W���I�ȕ��@�ɂ��TACE��̐������Ԃ̒����l��19.4�����A3�N�E�T�N��������40%�E32%�ƕ���Ă��܂��B
�Ö@
TACE�ŃR���g���[������ȑ��������̑��ȊO�ɓ]�ڂ�����悤�ȏꍇ�́A�Ö@�̓K���ɂȂ�܂��B���������т邽�߂Ɏ���ɓ���������u���ǐV���v��j�Q���镪�q�W�I��i�\���t�F�j�u�A�����o�`�j�u�A���S���t�F�j�u�A�����V���}�u�A�J�{�U���`�j�u�j��A����Ɖu�Ɋ֘A����Ɖu�`�F�b�N�|�C���g�j�Q�܁i�f�����o���}�u�j����ѕ����̋@����g�ݍ��킹�����p�Ö@�i�A�e�]���Y�}�u�{�x�o�V�Y�}�u�A�f�����o���}�u�{�g���������}�u�j�̗L�p�������̐��N�ő������Ŏ�����A�̍זE���̖Ö@�͑傫���l�ς�肵�Ă��܂����B
���q�W�I��ɂ́A�������E����E�`���A�E�����E�葫�̔S����Q�Ȃǂ̕���p�A�܂��A�Ɖu�`�F�b�N�|�C���g�j�Q��ɂ́A�����E�����A�b��B�@�\��Q�̑��A�Ԏ����x���≺���́E���t�@�\��Q�A�T�^���A�a�Ȃǂ̕���p����r�I���p�x�Ɍ����邽�߁A���ӂ��K�v�ł��B
�ȉ��ɁA�̍זE���ɑ���Ö@�̃A���S���Y���������܂��B
�Ö@�A���S���Y��
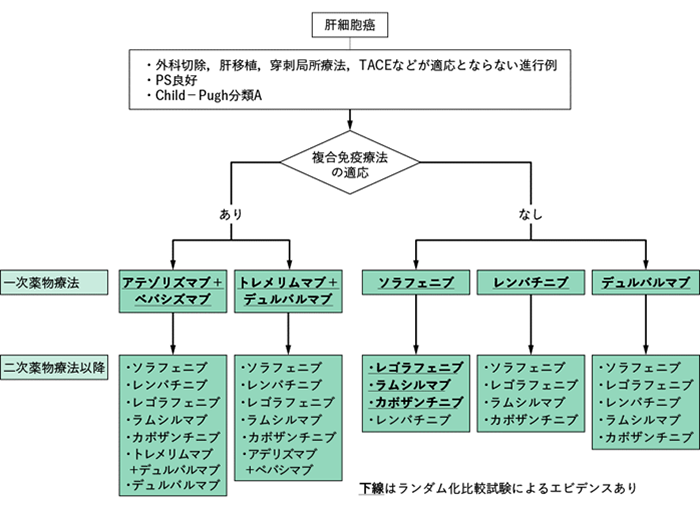
�i�̊��f�ÃK�C�h���C��2021�i2023�N5�������Łj���, ���{�̑��w��쐬, ���{�����Êw��HP���]�ځj
- �Ö@�̐���
�V�K�Ö@�̓o��ɂ��ABCLC���ނɂ��i�s���̗\��́A�̋@�\���ǍD�ȏꍇ�A�����Â�4-8�������x�ł��������̂��A�ŋ߂̕ł�13-19�������x�܂ʼn������Ă��Ă��܂��B
�ȉ��ɑ�\�I�ȖÖ@�Ɋւ���Տ������̐��сi#�͋ߔN�̗Տ������ɂ�����ΏƌQ�Ƃ��Ă̐��сj�������܂��B
| ���W������ | ���Ö@ | �Տ���������* | ||
|---|---|---|---|---|
| �t�� ���� |
�������������� �i�����l**�j |
�S�������� �i�����l**�j |
||
| �ꎟ���� | ||||
| �\���t�F�j�u | �A������ | 5% | 4.1���� | 13.8���� |
| �����o�`�j�u | �A������ | 19% 18% |
8.9���� 8.1���� |
13.6���� 19.0���� |
| �A�e�]���Y�}�u�{�x�o�V�Y�}�u | 3�T�Ԗ��ɓ_�H | 30% | 6.8���� | 19.2���� |
| �f�����o���}�u�{�g���������}�u(T) | 4�T�Ԗ��ɓ_�H (T�͏���̂݁j |
20% | 3.8���� | 16.4���� (4�N25%) |
| �f�����o���}�u | 4�T�Ԗ��ɓ_�H | 17% | 3.7���� | 16.6���� |
| ���Èȍ~ | ||||
| ���S���t�F�j�u | 1�R�[�X4�T�� 1-21���ڂɓ��� |
7% | 3.2���� | 10.6���� |
| �����V���}�u | 2�T�Ԗ��ɓ_�H | 5% | 2.8���� | 8.5���� |
| �J�{�U���`�j�u | �A������ | 4% | 5.2���� | 10.2���� |
*�Տ������̐��т́A�Ώۂ⎞��w�i�Ȃǂ̏������قȂ邽�߁A���̐��l�������đ��݂̐��т��r���邱�Ƃ͂ӂ��킵������܂���B�������͊e�����̗l�X�ȃf�[�^����a�Ԃɉ��������Ö@���ʂɌ������Ă���A���̈ꗗ�\���ȂĎ��Ö@�����肵�Ă͂���܂���B
**�����l�F�Ώێ҂�50%�����̒l������/�����l�B���ʂɂ͌l��������܂��B�܂��A�����l���Z���Ă������̐��������������ꍇ������A�����l�݂̂Ō��ʂ𑪂邱�Ƃ��K�Ƃ͂����܂���B
�����̐V�K�Ö@���K�����擾����Ɏ������Տ������́A�]���̕W�����Â������\���t�F�j�u�Ƃ̔�r�����A���Èȍ~�̓v���Z�{�i�U�����Áj�Ƃ̔�r�����ł���A�V�K���Ö@�ǂ������Ȋw�I�ɔ�r����悤�ȗՏ��������s���Ă��Ȃ����߁A�����̐V�K��܂̎g��������A�V�K��܂̎��Ì�ɕʂȖ�܂�p�����ꍇ�̐��сA���^���ȂǁA����𖾂��ׂ��ۑ肪�R�ς��Ă��܂��B
�܂��A�L�]�ȕW�����Â����������Ƃɂ��A�]���ATACE�������Ȃ��Ȃ������BCLC���ނ̐i�s���iTACE�s���j�œ�������Ă����Ö@���ABCLC���ނɂ�钆�Ԋ��̂����ATACE�����܂�����Ȃ��Ǝv�����ԁiTACE�s�K�j�ɂ��p������悤�ɂȂ����A�Ö@�̒�����ɁA�Ǐ��Ɏc�������ᇂɑ���TACE��RFA, ��p�Ȃǂ�g�ݍ��킹��V���Ȏ��Ð헪���o�ꂵ�Ă��܂��B
- �Q�m�����
�ߔN�A����ɑ���V���Ȏ��Ð헪�Ƃ��āA�����`�q�p�l���������̃Q�m�������ɂ�肪��̌����ƂȂ��`�q�ُ�肵�A�����W�I�Ƃ������q�W�I��𓊗^����A����Q�m����Â����ڂ���Ă��܂��B�̍זE���ł́A�e�������[�[��`�q�iTERT�j�ATP53�A���B�╪���Ɋւ��WNT�o�H�̈�`�q�iCTNNB1, AXIN1, APC�j�Ɉ�`�q�ُ�𑽂��F�߂܂����A2024�N3�����_�ŁA�����̈�`�q�ُ��W�I�Ƃ����g�p�\�Ȗ�܂͂���܂���B
����A2024�N3�����݁A�����`�q�p�l���������ňȉ��̈�`�q�ُ킪���������ꍇ�A�����ɂ�炸�A�ȉ��̖�܂��ی��f�É��Ŏg�p�\�ł��B�����A�̍זE���ł����ُ̈킪�����邱�Ƃ͔��ɂ܂�ł��B
- ���p�x�}�C�N���T�e���C�g�s���萫�iMSI-High�j��L����Ō`����E������ᇈ�`�q�ψٗʁiTMB-High�j��L����Ō`����F�y���u�����Y�}�u�i�Ɖu�`�F�b�N�|�C���g�j�Q��A�RPD-1�R�̖�j
- NTRK�Z����`�q�z���̌Ō`����F�G�k�g���N�`�j�u�A�����g���N�`�j�u�iTRK�j�Q��j
- BRAF��`�q�ψق�L����Ō`����F�_�u���t�F�j�u�iBRAF�j�Q��j�{�g�����`�j�u�iMEK�j�Q��j
���ː��Ö@
�̍זE���ɑ���W���I�ȋǏ����Â͎�p��RFA�ł����A�����̎��Â�����ȏꍇ�ɂ́A���ː����Â��I�����ɂȂ�܂��B5cm�ȉ��̊̓��Ǐ��a�ςɑ��ẮA����ʂ�X����5����x�̒Z���ԂŏW���I�ɏƎ˂����ʕ��ː�����(SBRT)���s���܂��BSBRT�͂���ɑ���3�����I�ɑ�����������ː����Ǝ˂��邱�Ƃɂ��A����ȍזE�ւ̉e����}���Ȃ���s���|�C���g�ł�������Â��邱�Ƃ��ł��鍂���x���ː����Â̂ЂƂł��B����A4cm����̓��Ǐ��a�ςɑ��ẮA2022�N��藱�q���i�z�q����d���q���j���Âɂ��ی����K�p�����悤�ɂȂ�܂����B���q�����Â͂���a�����ʂ��W�������邱�Ƃ��\�Ȏ��Âł����A�����ǂɋߐڂ���ꍇ�ȂǁA����̕��ʂɂ���Ă͎��Âł��Ȃ����Ƃ�����܂��B
���ː����Â̕���p�́A�}�����ɂ͌��ӊ��A�q�C��H�~�s�U�����O����܂����A���ÏI���ƂƂ��ɉ��P���Ă����܂��B���ÏI����A�ʏ퐔�����ȍ~�Ɍ����ӊ��̕���p�Ƃ��āA�_���n�̋���ɂ�鉩�t�A�̋@�\��Q�Ȃǂ��������܂��B
�x���Ö@
�̍זE���ɑ���Ö@�͒ʏ�Child-Pugh����A-6�_�܂łɍs���AB-7�_�ȏ�ł̈��S������ʂ͕s���ł��B�̋@�\���������Ă���ꍇ�ɂ́A���Âɂ��̋@�\������Ɉ������A�]�����k�߂Ă��܂��\���������Ȃ邽�߁A����ɑ��鎡�Â͂����߂ł��܂���B�ɂ݂Ȃǂ̏Ǐ�ɘa��ړI�Ƃ������Â�A�ނ��݂╠���̎��ÂȂǂ̊̋@�\�ێ���ړI�Ƃ������Â��s���܂��B
�Ĕ��̐f�f�Ǝ���
��p��W�I�g�ĎܗÖ@��̍Ĕ��́A���̑������Ăъ̑����ɔ������܂��B���̏ꍇ�A�ӂ��̏��l�����܂��B�ЂƂ͑��̂����Ɠ��l�̓]�ڂŁA�����ЂƂ͐V���Ȕ�����i�����S�������Ƃ����܂��j�ł��B�̍זE���̑����͊̉��E�̍d�ς��甭�����܂����A�̉��E�̍d�ς͂�������������̓y��ł��B����̃^�l���������܂��Ă���Ԓd����A���X���肵�ĉԊJ�����Ƃ�����C���[�W���Ă��������B
���̂悤�ɁA�̍זE���͑��̂����Ɣ�ׂĂƂĂ��Ĕ����₷���A�����I�Ȏ��Â̂��Ƃł��AAFP�Ȃǂ̎�ᇃ}�[�J�[��CT������3�4�������ƂɌJ��Ԃ��A�����ɂ킽���čĔ����������Ă����܂��B
�����I���Â̂��Ƃ̏h���I�ȍĔ����Ȃ�Ƃ��\�h���邱�Ƃ͂ł��Ȃ������N�������d�˂��Ă��܂����m���ɍĔ���\�h���鎡�Ö@�͖����J������Ă��܂���B
�̓��̍Ĕ����������ꂽ��A�͂��߂Ĕ������ꂽ�Ƃ��Ɠ������Ö@�I���̎菇�Ŏ��Â����߂܂��B�����������Ď�p���\�ł��B����A�̊O�̍Ĕ��͖��炩�ȓ]�ڂŁA����זE���S�g�������Ă���Ƃ݂Ȃ����ł��̂ŁA�Ö@�̑ΏۂƂȂ�܂��B
������
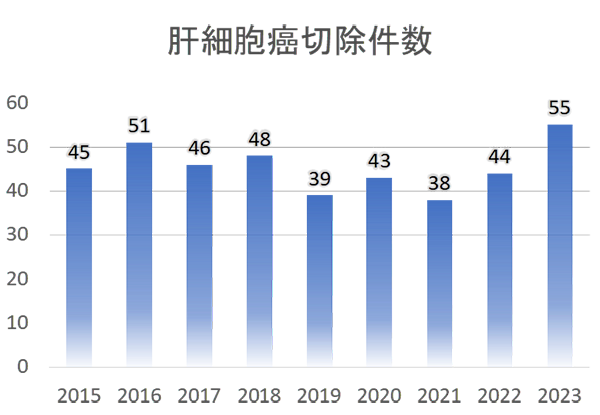
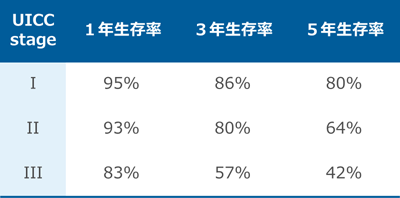
�������̑����́A�����I���Â̂��Ƃ�5�N�قǂōĔ����Ȃ��Ȃ�A5�N���Ĕ��Ȃ�قڎ����ƍl���܂��B�������A�̍זE���͊̉��E�̍d�ς��������V���Ȕ����N����܂�����A���N�����Ă������Ƃ������t�͎g���ɂ��������ł��B�ڈ��Ƃ���5�N�������́A��p�Ö@��40-70%�A�o��I�Ǐ��ĎܗÖ@��30-60���A���Ǎǐ����w�Ö@��10-30�����炢�ł��B





![�}�F�咰����̓]�ڏp�㐶����](images/index_img08.png)

