
胃外科
胃がん通信バックナンバー
※ こちらのページは医療機関向けとなりますが、一般の方もご覧いただけます。
- 2026年度 第一号
- 2025年度 第一号
- 2024年度 第二号
- 2024年度 第一号
- 2023年度 第二号
- 2023年度 第一号
- 2022年度 第二号
- 2022年度 第一号
- 2021年度 第一号
- 2020年度 第二号
- 2020年度 第一号
- 2019年度 第二号
- 2019年度 第一号
- 2018年度 第二号
- 2018年度 第一号
- 2017年度 第二号
- 2017年度 第一号

胃がんグループはチーム医療で患者さんに最適な治療を提供します
平素より患者さんをご紹介頂きまして誠にありがとうございます。胃がんにつきましては、ピロリ菌除菌の普及によって今後患者数が減少していくことが予想される中、当院ではカンファレンスやキャンサーボードを通して患者さん一人ひとりに迅速かつ最適な治療を提供できるよう、内視鏡科・外科・化学療法科が緊密に連携し、日々診療にあたっております。そして、可能な限りご紹介頂いた患者さんのご期待に応えたいと思っております。
がん研有明病院への患者さんのご紹介をお考えの際は、どうぞお気軽にお問い合わせください。
(胃外科部長 布部 創也)
胃外科スタッフ紹介
-

佐野武
病院長 -

布部創也
部長 -

大橋学
手術部長 -

入野誠之
医長 -

速水克
医長 -

幕内梨恵
副医長 -

李基成
副医長
上部消化管内科スタッフ
-

後藤田卓志
部長 -

平澤俊明
胃担当部長 -

由雄敏之
食道担当部長 -

石山晃世志
副部長 -

堀内祐介
医長 -

吉水祥一
医長 -

山本 浩之
副医長
消化器化学療法科スタッフ紹介
-

山口研成
部長 -

陳勁松
外来化学
療法部長 -

篠崎英司
副部長 -

大木暁
副部長 -

若槻尊
医長 -

小倉真理子
副医長 -

大隅寛木
副医長 -

福岡聖大
副医長 -

宇田川翔平
副医長 -

下嵜啓太郎
副医長
化学療法トピック
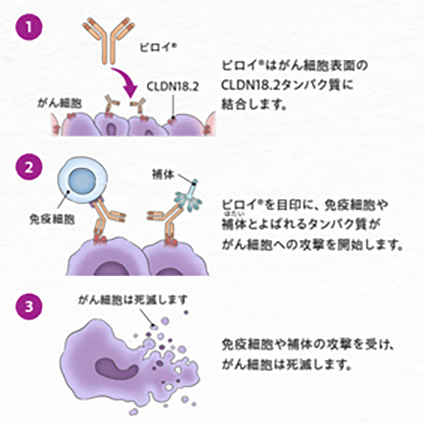 昨年5月の胃がん通信に掲載したゾルべツキシマブが「クローディン(Claudin)18.2陽性の治癒切除不能な進行・再発の胃がん」を対象に、ビロイ点滴静注用100mgとして承認されました。クローディンは、細胞間の緊密な結合を形成する膜貫通型タンパク質です。正常細胞では細胞表面には出現しておりませんが、がん細胞が異常増殖する際に細胞表面に出現します。ゾルベツキシマブはクローディン18.2に結合し、抗体依存性細胞障害や補体依存性細胞毒性を介して胃がん細胞の増殖を抑制します(右図)。
昨年5月の胃がん通信に掲載したゾルべツキシマブが「クローディン(Claudin)18.2陽性の治癒切除不能な進行・再発の胃がん」を対象に、ビロイ点滴静注用100mgとして承認されました。クローディンは、細胞間の緊密な結合を形成する膜貫通型タンパク質です。正常細胞では細胞表面には出現しておりませんが、がん細胞が異常増殖する際に細胞表面に出現します。ゾルベツキシマブはクローディン18.2に結合し、抗体依存性細胞障害や補体依存性細胞毒性を介して胃がん細胞の増殖を抑制します(右図)。
FOLFOXもしくはCAPOXとの併用で使用可能となります。HER2陰性胃がんの約38%がクローディン18.2陽性と診断されており、比較的多くの患者さんが治療対象となります。一方でクローディン18.2陽性例の13-22 %がPD-L1陽性例であり、抗PD-1抗体の治療対象となります。この集団を対象にした国際共同第III相試験であるILUSTRO試験においてFOLFOX+ゾルベツキシマブ+ニボルマブ併用療法が検証されております。またクローディン18.2を標的とした薬剤は続々と開発されており、当院先端医療科でも早期臨床試験が行われております。
(消化器化学療法科 福岡 聖大)
胃内視鏡領域のトピック
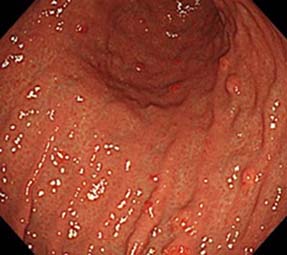
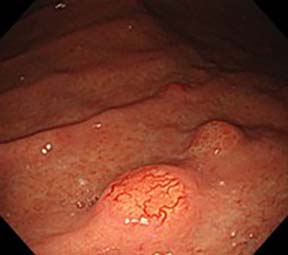
胃の神経内分泌腫瘍(NET)はRindiらの報告以来、疾患背景によりType I〜IIIに分類されてきました。しかし近年いずれにも分類できない、壁細胞機能不全症を背景とした症例が報告されています。現在のところ国内外で9例の論文報告があり、既報2例と未報告2例が当院で、当院診断補助のもと、既報の1例が関連病院で診断されています。胃酸は胃底腺の壁細胞から分泌され、壁細胞に存在するproton pump (H+/K+-ATPase) が関与しますが、そのproton pumpの機能不全により胃酸分泌が減少し、胃内pHが上昇します。続いてnegative feedback機構により幽門腺領域のGastrin細胞が増加し高ガストリン血症をきたすことで胃底腺領域のEnterochromaffin-like cells (ECL細胞)の過形成および腫瘍化が誘発されます。原因としてproton pumpの構成蛋白をコードするATP4Aの変異が報告されており、生来胃酸が出ない疾患ですが基本的に無症状なので検診等で多発隆起性病変を契機に偶発的に発見されます。鑑別診断としてRindi分類Type Iである自己免疫性胃炎がありますが、壁細胞機能不全症では内視鏡的にも病理学的にも萎縮や炎症を伴わないことが特徴的です。
この様な症例を当院から報告できているのも先生方からの沢山のご紹介あってのことです。今後も胃がん領域をリードするエビデンスを構築するべく、チーム一丸となって邁進します。引き続きよろしくお願いいたします
文献:1) Ishioka M, et al. Gastrointest Endosc. 2019.
(上部消化管内科 渡邊 昌人)
Dr.平澤の内視鏡クイズ
40歳代女性.既往:なし
食後の腹部膨満感があり、近医を受診。上部消化管内視鏡検査で胃炎と診断され、生検結果はGroup1であった。その後、3つの医療機関で内視鏡検査を受けたが、診断がつかず、生検結果もGroup1であった。
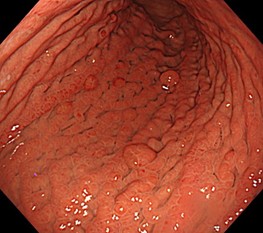
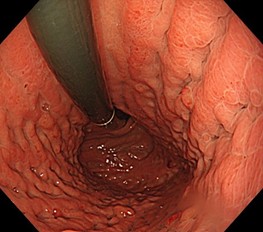
胃体部には伸展不良、壁硬化像、皺壁腫大が認められ、典型的なスキルス胃がんである。スキルス胃がんは一般的に粘膜内で発生し、すぐに粘膜下層に浸潤し、粘膜下層以深でさらに浸潤していく。そのため、生検でがんが検出されないことも珍しくない。生検は、がんが露出している可能性のある粘膜の陥凹、びらん、潰瘍部位で行うべきである。NBI拡大観察が有用な場合もある。本症例では、びらんからの生検でがんが検出された。しかし、粘膜内にがんが全く露出していない症例もあり、その場合はボーリング生検、EMR、審査腹腔鏡などを行い、早急に診断を下す必要がある。
スキルス胃がんは診断が難しく、進行が速いため、疑われる場合は速やかにがん研有明病院へのご紹介をご検討ください。


美麗な内視鏡画像と手技の動画を豊富に 掲載し,がんを見逃さないポイントが一目瞭然!

胃外科トピック
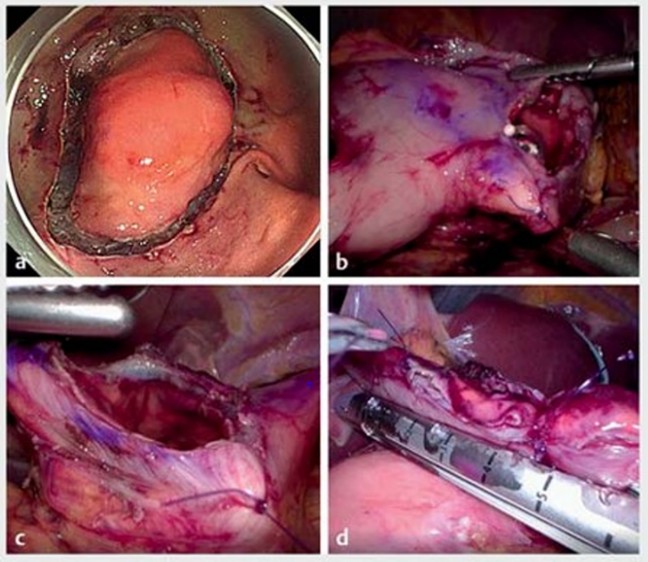
腹腔鏡内視鏡合同手術 (LECS) は胃上皮下病変 (SEL) に対する治療法として、当院で開発された手技です (図1)。現在では、最小限の局所切除法として、胃のみならず他臓器でも応用され、アジア諸国でも普及しています。胃SELに対するLECSの有効性と安全性についての報告は多数ありますが、悪性である消化管間葉系腫瘍 (GIST) に対するLECSの腫瘍学的安全性は明確ではありませんでした。そのため、2006年から2020年にかけて胃GISTに対して当院でLECSを施行した患者さんを対象に、手技の完遂率、合併症率、予後について検討を行いました。結果は、99.1%の高い完遂率と、2.8%の低い合併症率が示され、胃GISTに対してのLECSの短期的な安全性が確認されました (表1)。さらに、LECSを施行した患者さんの5年全生存率 (OS) および疾患特異的生存率 (DSS) はそれぞれ99%と100%であり、良好な長期成績が得られました (図2)。 本検討により、LECSが胃GISTの安全で効果的な治療選択肢であることが示されました。ただし、LECSの適用は腫瘍の位置や大きさによって決定されるため、その腫瘍の特性を十分に理解した上で行うことが重要であると考えられます。
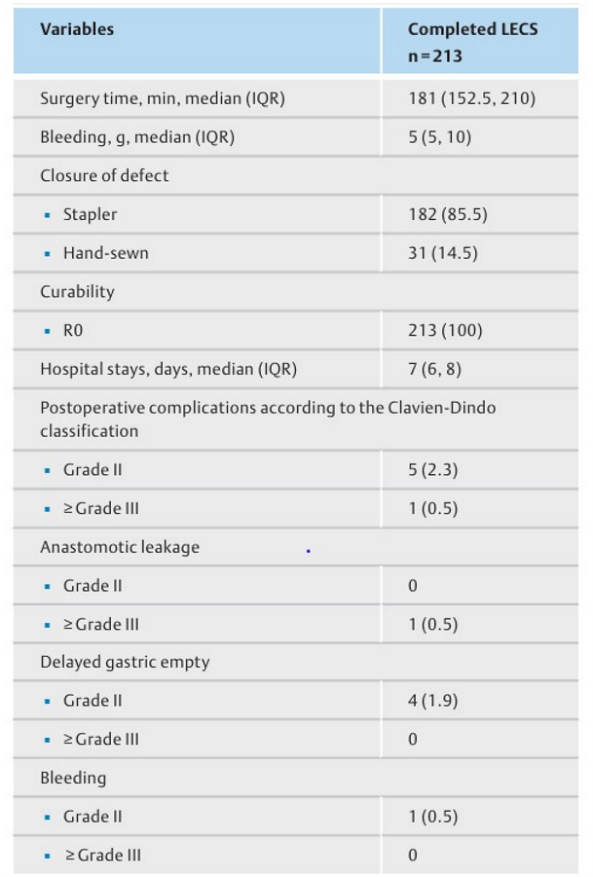
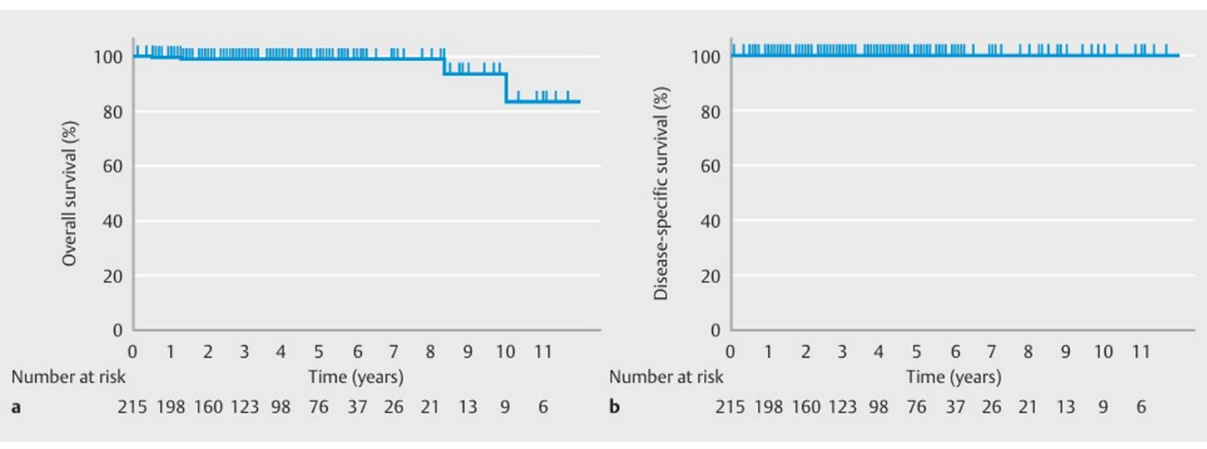
文献:1) Harada H, et al. Endosc Int Open. 2022.
(胃外科 原田 宏輝)
がん研有明病院では、先生方からのご紹介に対し、迅速に対応できるようにご紹介専用電話を開設しております。お困りの患者さんがいらっしゃいましたら、いつでもご連絡ください。
 <ご紹介連絡先>診療予約室
<ご紹介連絡先>診療予約室
電話:03−3570−0506(直通:医療機関専用)
FAX:03−3570−0254
受付時間:平日 午前8時30分〜午後4時30分



